结晶
结晶是一种自然过程,当材料从液体中凝固,或者从液体或气体中沉淀出来时,就会发生结晶。这个过程可以通过引起物理变化(如温度变化)或化学变化(如酸度)来进行。结晶过程是根据所涉及分子的大小和形状以及它们的化学性质进行的。晶体可以由一种原子、不同种类的离子,甚至是蛋白质等大分子组成。一些大分子很难通过结晶过程,因为它们的内部化学不是对称的或与自身相互作用以避免结晶。
晶胞被称为晶体的最小单位。它是可以连接更多单元的原子或分子的基本形式。将其视为儿童的积木,可以将其他积木加入其中。结晶继续进行,就好像这些块在各个方向上都连接在一起。一些材料形成不同形状的晶体,导致各种晶体的形状、大小和颜色变化很大。

结晶类型
冷却结晶
将饱和溶液在 30°C 冷却至 0°C,当水水合后沉淀出大晶体块时,就会发生沉淀。
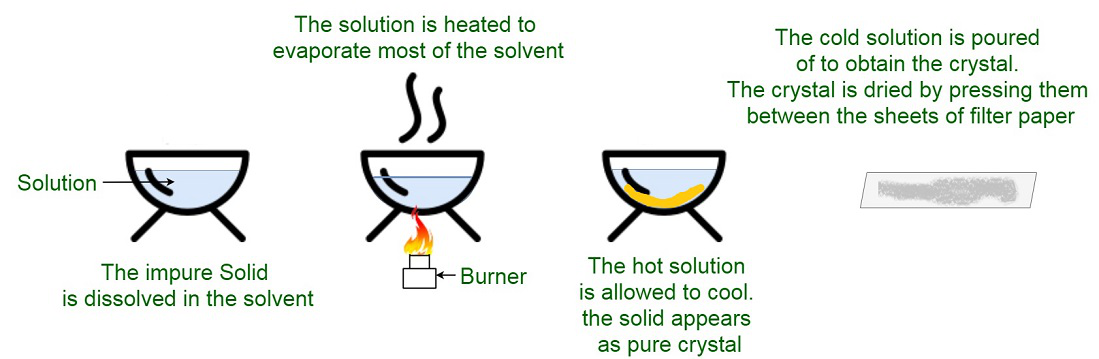
蒸发结晶
在恒定温度下,通过将溶质浓度提高到溶解度阈值以上来沉淀晶体。使用蒸发技术增加溶质/溶剂质量比。
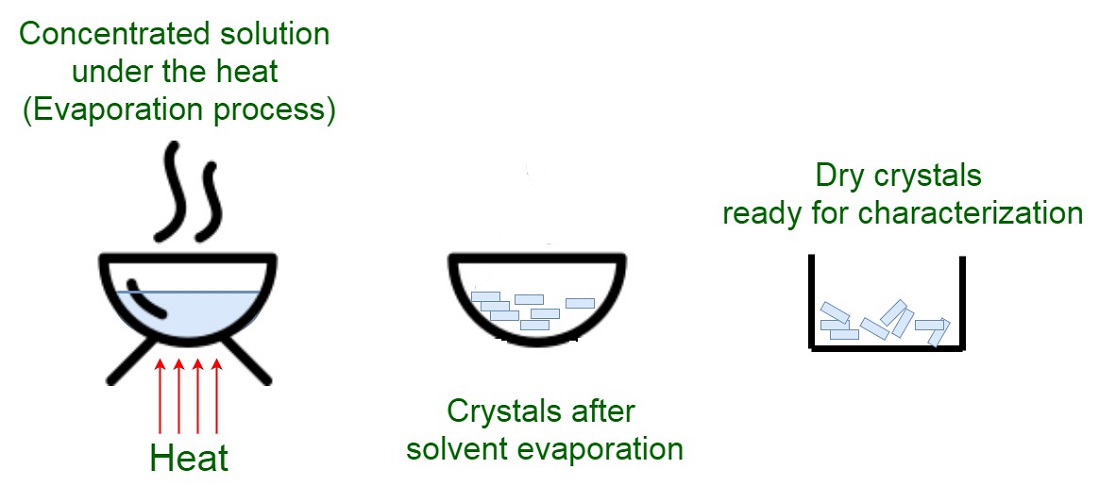
影响结晶的因素
- 存在另一种物质:从水溶液中结晶的氯化钠产生立方晶体。如果氯化钠从含有少量尿素的溶液中结晶出来,所得晶体将具有八面体面。
- 溶剂:结晶优选溶解度适中的溶剂。苯的存在有助于晶体生长。避免使用高挥发性溶剂。
- 成核:晶体最初是通过“成核事件”形成的。微晶成核后必须生长。成核位点是晶体形成所必需的。过多的成核位点导致较小的平均晶体尺寸。
- 晶体生长:晶体通过溶质分子有序沉积在预先存在的晶体表面上而生长。随着时间的推移缓慢变化的环境促进了晶体的生长。使晶体生长容器远离机械搅拌源(例如振动)。远离真空泵、抽油烟机、门、抽屉等设置。
- 冷却速率/时间:质量晶体在接近平衡的条件下随着时间的推移生长得最好。时间越长,晶体越好。较快的结晶不如慢结晶。结晶速度越快,晶体质量越低的几率越高。
结晶的重要性:
- 药物纯化
- 提高药物的生物利用度,选择最稳定的形式
- 结晶粉末易于处理、稳定、具有良好的流动性并具有吸引人的外观。
结晶的应用
结晶是小分子药物制造中几乎所有过程的关键组成部分。它在加工和药物开发中都是必不可少的。由于固体材料的特性(多晶型)会显着影响工艺或产品的顺应性和效果(例如溶解速率),因此通过结晶监测和控制各种应用中固体的分离是最重要的。
所以结晶用于:
- 药物纯化
- 更好的加工特性
- 易于处理
- 提高物理稳定性
- 持续释放
- 提高生物利用度
- 有机和无机 API 的制备 8- 从盖仑提取物中分离 API
- 高产量生产纯原料药
结晶理论:
结晶过程的三个主要阶段是:
- 溶液超饱和:可以通过三种方式进行:加热溶液、冷却溶液、盐析。
- 成核:这发生在几个步骤中。在它们的随机运动过程中,原子/分子/离子将彼此靠近并形成称为簇的聚集体。这些集群将结合形成一个胚胎。在这个阶段,只有晶格形成开始。这个胚胎结合形成核。由晶核形成晶体。
- 晶体生长:一旦晶体形成,晶核形成停止,晶体生长开始。
结晶过程
结晶过程包括两个主要事件。一种是成核,另一种是晶体生长,它们都由热力学性质和化学性质驱动。成核是分散在溶剂中的溶质分子或原子开始聚集成簇的主要步骤,这些簇在目前的操作条件下变得稳定。这些稳定的簇构成了原子核。因此,星团必须达到临界尺寸才能成为稳定的原子核。在成核阶段,原子或分子以定义晶体结构的定义和周期性方式排列。
晶体生长是指能够达到临界簇尺寸的核尺寸的增加。许多化合物具有结晶能力,其中一些具有不同的晶体结构,这种现象称为多晶型现象。某些多晶型物可能是亚稳态的,这意味着尽管它不处于热力学平衡,但它在动力学上是稳定的,并且需要一些能量输入来启动平衡相的变化。
结晶的例子:
下面列出了一些常见的结晶示例:
- 水结晶形成冰块和雪。
- 将蜂蜜放入罐中并暴露在适当条件下时的结晶。
- 石笋和钟乳石的形成(特别是在洞穴中)。
- 宝石晶体的沉积。
结晶有什么好处?
下面列出了结晶的主要优点。
- 通过结晶过程可以从一个单一步骤获得高纯度的产品。
- 结晶形成的干品可直接包装储存。
- 该过程的能量需求和操作温度相对较低。
示例问题
问题 1. 什么是风化?
回答:
Efflorescence: Crystalline hydrated salts which on exposure to the atmosphere lose their moisture (water of crystallisation) partly or completely to the atmosphere and change into the amorphous state. Examples: Washing soda (Na2CO3.10H2O), Glauber salt (Na2SO4.10H2O).
问题 2. 定义结晶水,举两个例子和它们的化学式?
回答:
The definite amount of water associated with hydrated crystals which is an integral part of the crystal is known as water of crystallisation.
Example:
- Blue vitriol CuSO4.5H2O
- Glaubler salt Na2SO4.10H2O
问题 3. 氯化钠的无水晶体是否含有水?含有结晶水的晶体与无水氯化钠晶体有何不同?
回答:
Anhydrous substance does not contain water molecule. These obtained from hydrated salts by carefully removing water of crystallization from them.
NaCl is an anhydrous salt but if some impurity like salts of group II is present, they absorb moisture from the air because they are hygroscopic substances that’s why NaCl looks moist. But it’s an anhydrous salt.
Let us take an example so that you will clear your concept about this,
CuSO4.5H2O + heat → CuSO4 + 5H2O
Blue White
(Salt with water of crystallization) (anhydrous salt)
问题 4. 命名一种十水合结晶盐。给出它的分子式。
回答:
Washing soda (Na2CO3.10H2O) is a decahydrate crystalline salt.
问题 5. 结晶和蒸发的区别?
回答: Crystallization EvaporationCrystallization is the process of formation of solid Crystals Precipitating from a solution, melt or more rarely deposited directly from a gas. Evaporation is a type of vaporization of a liquid that occurs only on the surface of a liquid. Is used when the soluble solid does not decompose upon strong heating Is used when the soluble solid contains water of crystallisation. Drawback: any soluble impurities may also be present after evaporation. Advantage: pure solid is collected in the form of crystals. Example: Seawater Evaporating and forming into clouds. Example: Dry Ice.
问题 6. 结晶和再结晶有什么区别?
回答:
Recrystallization is done to crystals formed from a crystallization method.
Crystallization is a separation technique. Recrystallization is used to purify the compound received from crystallization.
问题 7. 结晶过程中溶液中的不溶性杂质如何去除?
回答:
Filtration is the process of separating small particles of solid matter from a liquid, by causing the liquid to pass through the pores of some substance, called a filter.
Insoluble impurities from solution during crystallization are removed by filtration as the insoluble solid particles passed through the filter.