碳氢化合物的分类
有机化学是处理含有碳原子和共价键(涉及原子之间共享电子的化学键)的有机化合物的反应、结构和性质(物理和化学)的化学分支。
任何仅由碳(C)和氢(H)原子组成的有机化合物称为碳氢化合物。碳原子结合在一起形成化合物的结构,氢原子以多种方式与其结合。石油和天然气主要由碳氢化合物组成。它们用作燃料和润滑剂,以及塑料、纤维、橡胶、溶剂、炸药和工业化学品的原材料。
Hydrocarbons are abundant in nature. They are found in trees and plants as well as fossil fuels, for example, in the form of carotenes, which are pigments found in carrots and green leaves. A hydrocarbon polymer, a chainlike molecule made up of numerous units linked together, makes up more than 98% of natural crude rubber. Individual hydrocarbons’ shapes and chemistry are mostly determined by the types of chemical bonds that connect the atoms of their constituent molecules.
什么是碳氢化合物?
Hydrocarbons are made of two words hydro and carbon, in which hydro represents hydrogen elements and carbon represents carbon elements, so hydrocarbons can be easily defined as compounds that are formed from hydrogen and carbon molecules only.
烃可以以直链和环状结构存在。这些碳氢化合物用于制造新材料的不同工艺。
烃分为四个子类别:烷烃、烯烃、炔烃和芳烃。烷烃、烯烃、炔烃和芳烃具有简单或中等复杂的结构。对碳氢化合物的研究可以揭示有关其他官能团的化学特性和制造的信息。
C x H y是这些物质的分子式。碳氢化合物可以在植物和树木中找到。例如,胡萝卜素是一种存在于绿叶和胡萝卜中的有机色素。碳氢化合物以不同的形式存在于自然界中,例如由原油、石油、煤油、液化石油气 (LPG)、压缩天然气 (CNG) 等组成的化石燃料都含有碳氢化合物。这意味着碳氢化合物是一种重要的能源。
碳氢化合物的性质:
- 碳氢化合物分子的熔点和沸点受分子大小的影响。因此,在室温下,某些碳氢化合物是气体,而其他碳氢化合物是液体或固体。
- 它们由强碳氢键组成。
- 分子具有很强的分子吸引力。
- 非极性是指碳氢化合物分子中不存在带相反电荷的侧面。因此,它们是极性化合物,不溶于水。另一方面,碳氢化合物具有排斥水的自然趋势。这就是地板蜡和其他相关产品含有它们的原因。
碳氢化合物的分类和种类
碳氢化合物以前被老科学家分类为脂肪族或芳香族。来源和特征用于对碳氢化合物进行分类。结果,发现脂肪或油的化学降解形成脂肪烃,而芳香烃包括植物提取物化学降解形成的组分。然而,我们现在根据碳氢化合物的结构而不是它们的来源对碳氢化合物进行分类。
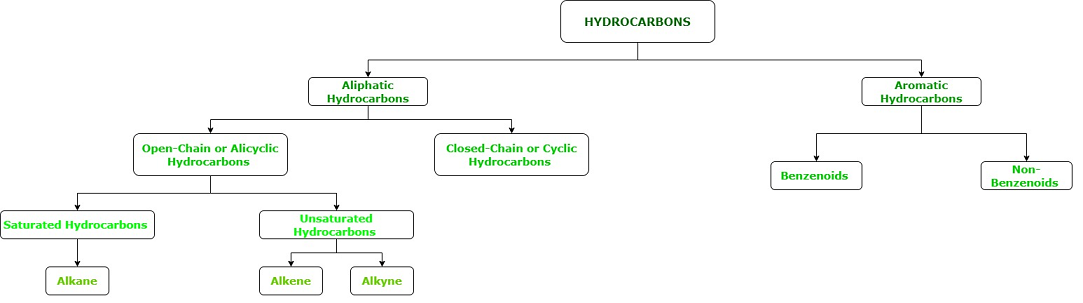
饱和烃
饱和烃被称为烷烃。这些碳氢化合物含有碳-碳和碳-氢的单键。这些碳氢化合物形成本质上开放的链结构。这些碳氢化合物不含任何双键或三键。饱和烃被称为最简单的烃。饱和烃的通式是C n H 2n+2 。

饱和烃(烷烃)的物理性质
- 饱和烃(烷烃)本质上是无色无味的。
- 烷烃是非极性分子。
- 烷烃的前 4 个成员以气相形式存在。从第五到第十七的接下来的十三个成员存在于液相中。
- 含有超过 18 个碳原子的烷烃本质上是固体。
- 烷烃中存在分子间范德华力。具有较强分子间范德华力的烷烃具有较高的沸点。
- 由于与上述相同的原因,烷烃的熔点遵循与沸点相似的趋势。也就是说,分子越大(其他条件相同),熔点就越高。
饱和烃(烷烃)的化学性质
- 加热时,烷烃与氧气反应并产生二氧化碳和水。让我们取烷烃的第一个成员甲烷 (CH 4 ) 并加热它。
CH 4 (气体) + 2O 2 (气体) → CO 2 (气体) + 2H 2 O(液体)
- 氢原子可以被氟、氯、溴、碘与卤素基团取代,形成新的化合物,这个过程称为卤化。卤化过程在有阳光的情况下发生。
CH 4 + Cl 2 → CH 3 Cl(氯甲烷)+ HCl
- 在异构化和重整过程中,直链烷烃在铂催化剂的存在下被加热。异构化将烷烃转化为支链异构体。烷烃经过重整变成环烷烃或芳烃,释放出氢气作为副产品。这两种方法都会增加物质的辛烷值。丁烷是最常见的异构化烷烃,因为它会产生大量具有高辛烷值的支链烷烃。
饱和烃(烷烃)的制备
烷烃可以通过多种方法制备,其中一些方法如下所述:
- 来自不饱和烃
不饱和烃是烯烃或炔烃,可以在催化剂(如镍)存在下通过添加氢气转化为烷烃,这种烷烃形成过程称为氢化。
C 2 H 4 (乙烯) + H 2 → C 2 H 6 (乙烷)
- 来自卤代烷
烷烃也可以通过卤代烷在锌的存在下与氢反应来制备。
CH 3 Cl + H 2 Zn → CH 4 (甲烷) + HCl
不饱和烃
不饱和烃是完全由碳和氢原子组成的有机分子,在两个相邻的碳原子之间具有双键或三键。烯烃是在两个相邻碳原子之间含有至少一个双键的烃,而炔烃是含有碳-碳三键的烃。饱和烃和不饱和烃具有不同的化学式,如下所示。
不饱和烃有两种类型:
- 烯烃
- 炔烃
烯烃:不饱和烃含有烯烃。烯烃是油形成化合物,因此这些被称为烯烃。这些烃包含碳-碳和碳-氢的单键以及至少一个双键。这些碳氢化合物还形成本质上开放的链结构。
烯烃的通式: C n H 2n

烯烃的物理性质
- 不饱和烃(烯烃)在自然界中是无色无味的,但乙烯具有甜味。
- 烯烃比同类烷烃具有更强的气味。
- 烯烃是极性分子。
- 物理状态由分子质量决定:最简单的烯烃,如相应的饱和烃,在室温下为气体。
- 烯烃的前 3 个成员以气相形式存在。
- 接下来从第四到第十七的十四个成员存在于液相中。
- 含有超过 14 个碳原子的烯烃本质上是固体。
- 这些具有高熔点和沸点。
烯烃的化学性质
- 烯烃具有进行加成反应的特性,因此它会添加氢分子以形成烷烃。
C 2 H 4 (乙烯) + H 2 → C 2 H 6 (乙烷)
- 氢原子可以被氟、氯、溴取代,即与卤素基团形成新的化合物,称为二卤化物,但碘除外,因为碘不发生加成反应。
C 2 H 4 (乙烯) + Br 2 → C 2 H 4 Br 2 (二溴乙烷)
烯烃的制备
烯烃可以通过多种方法制备,其中一些方法如下所述:
- 来自炔烃:不饱和烃(烯烃)可以通过在催化剂(如木炭)存在下添加氢气由炔烃制备,这种催化剂也称为 Lindlar 催化剂。
C 2 H 2 (乙炔) + H 2 Pd/C → C 2 H 4 (乙烯)
- 由卤代烷:烯烃也可以由卤代烷制备,方法是在溶解在醇中的钾盐存在下加热烯烃,以从卤代烷中去除卤素分子。
C 2 H 5 Cl → C 2 H 4 (乙烯)
炔烃:不饱和烃也含有炔烃。这些碳氢化合物包含碳-碳和碳-氢的单键以及两个碳原子之间的至少一个三键。这些碳氢化合物还形成本质上开放的链结构。炔烃系列的第一个成员是乙炔,也称为乙炔。
炔烃的通式: C n H 2n-2

炔烃的物理性质
- 不饱和烃(炔烃)在自然界中是无色无味的,但有气味的乙炔除外。
- 炔烃是极性分子。
- 炔烃的前 3 个成员以气相形式存在。
- 接下来从第四到第十一的八个成员存在于液相中。
- 含有超过 11 个碳原子的炔烃本质上是固体。
炔烃的化学性质
- 炔烃也表现出像烯烃一样的加成反应,因为炔烃具有三键,因此它们倾向于加成两个氢、卤素、卤化氢分子以形成不同的化合物。
- 炔烃不与水反应。
- 炔烃显示聚合意味着它们可以形成长链碳分子。
炔烃的制备
炔烃可以通过多种方法制备,其中一些方法如下所述:
- 从电石中:可以通过向电石中加入水来制备炔烃,这将导致氢氧化钙和炔烃(例如乙炔)的形成。
CaC 2 + 2H 2 O → Ca(OH) 2 + C 2 H 2 (乙炔)
- 从连位二卤化物中:炔烃可以从连位二卤化物中制备,方法是将它们与醇钾反应,从二卤化物中消除一分子卤素,形成烯基卤化物,然后将其还原为炔烃。
芳烃
芳香一词来自芳香一词,意思是令人愉快的气味,因此芳香化合物具有令人愉快的气味。这些碳氢化合物也称为芳烃。大多数芳烃含有苯环,因此被称为苯类。有一些芳烃不含苯环,因此也称为非苯类。

芳香烃的物理性质
- 这些化学物质是芳香的(共振赋予的额外稳定性)
- 在这些化合物中,碳氢原子比相对较高。
- 芳香烃以气相和液相存在。
- 芳香烃本质上是无色的。
- 芳烃不溶于水。
芳香烃的化学性质
- 芳烃能够进行亲电取代反应。
- 在某些条件下,这些碳氢化合物还可以发生加成和氧化反应。
- 当芳烃燃烧时,它们会产生黄色的煤烟。
芳烃的制备
- 苯酚的还原:芳烃说苯可以通过锌粉还原苯酚来制备。
C 6 H 6 OH (苯酚) + Zn → C 6 H 6 (苯) + ZnO
- 芳香酸的脱羧:芳香烃称苯可通过加热苯甲酸钠盐而制得。
C 6 H 6 COONa + NaOH CaO → C 6 H 6 (苯)+ Na 2 CO 3
碳氢化合物的用途
- 碳氢化合物在油漆中用作溶剂。
- 这些也用于油脂和润滑剂行业。
- 不同类型的药物使用碳氢化合物进行制备。
- 碳氢化合物用于合成不同类型的聚合物。
- 燃料主要由碳氢化合物组成。
- 天然气主要由甲烷组成。
- 乙烷和丙烷要么转化为合成气,要么转化为乙烯和丙烯。
示例问题
问题1:为什么不存在Methene?
回答:
Methene does not exist as for alkenes to make there should be one carbon-carbon double bond so two carbon atoms are needed and this is the reason that methene which contains only a single carbon atom does not exist.
问题 2:什么是 Huckel 规则?
回答:
Aromatic compounds are compounds that contain one benzene ring, benzene rings contain electrons which should follow a rule called the Huckel rule. The presence of (4n+2) pi electrons in the ring is the Huckel rule.
问题 3:什么是臭氧分解?
回答:
Ozonolysis is the process of the addition of ozone molecules to the alkene to form ozonide, this process is useful in investigating the location of the double bond in alkenes.
问题 4:什么是热解?
回答:
Decomposition of higher alkanes into lower alkanes by the effect of heat is called pyrolysis, another name of pyrolysis is cracking.
问题5:为什么没有甲乙炔?
回答:
Methyne does not exist as for alkynes to make there should be one carbon-carbon triple bond so two carbon atoms are needed and this is the reason that methyne which contain only a single carbon atom does not exist.