一氧化硫和二氧化硫
硫是丰富的、多价的和非金属的。在常温下,元素硫为亮黄色结晶固体。按质量计算,硫是宇宙中第十丰富的元素,也是地球上第五丰富的元素。地球上的硫通常以硫化物和硫酸盐矿物的形式存在,而偶尔以纯天然形式存在。今天几乎所有的元素硫都是从天然气和石油中去除含硫杂质的副产品。该元素最重要的商业应用是制造用于硫酸盐和磷酸盐肥料的硫酸,以及其他化学过程。
Sulphur is a chemical element with the symbol S and atomic number 16.
许多硫化合物是有气味的,有机硫化合物是加臭天然气、臭鼬气味、葡萄柚和大蒜气味的原因。腐烂的鸡蛋和其他生物过程的气味是由硫化氢引起的。所有生命都需要硫,然而,它几乎总是以有机硫化合物或金属硫化物的形式存在。有机硫化合物包括三种氨基酸(半胱氨酸、胱氨酸和蛋氨酸)和两种维生素(生物素和硫胺素)。硫是所有生物必需的大量营养素,也是代谢功能所需的关键化学成分之一。让我们研究一下硫的两种氧化物。
一氧化硫
Sulfur monoxide (SO) is an inorganic chemical. It only exists as a dilute gas phase. It transforms to S2O2 when concentrated or condensed (disulphur dioxide). It has been discovered in space, but it is rarely seen intact on Earth.
SO的形成
放电在二氧化硫和硫蒸气的低压组合中产生不稳定的无色气体;冷却后冷凝成橙红色固体,缓慢分解为硫和二氧化硫。
SO的结构和键合
SO 分子具有三重基态,这意味着每个分子都有两个不成对的电子。气态 S 2 O、SO 2和 SO 3中的 SO 键长度为 148.1 pm,与低硫氧化物中的 SO 键长度相似,但比气态 S 2 O 中的 SO 键长度长、 SO 2和 SO 3 。分子被近红外辐射激发到单重态(没有不成对的电子)。单线态被认为比基态三线态更具反应性,就像单线态氧被认为比三线态氧更具反应性一样。
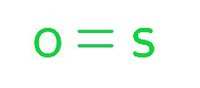
一氧化硫结构式
SO的产生和反应
- 在有机合成中使用挤出 SO 作为试剂的分子已集中在 SO 作为试剂的生产上。相对简单的分子环亚砜的分解,以及更复杂的分子,例如三硫化物,C 10 H 6 S 3 O,都是例子。
C 2 H 4 SO → C 2 H 4 + SO
- SO 分子在热力学上不稳定,首先变为 S 2 O 2 。 SO 插入烯烃、炔烃和二烯烃中形成硫杂丙环,分子具有三元硫环。
SO的安全措施
由于它在我们的大气中稀有且稳定性低,因此很难充分估计其风险。然而,当它被冷凝和压实时,它会产生二氧化硫,这种二氧化硫具有致命性和腐蚀性。这种分子也非常易燃(类似于甲烷)并释放二氧化硫,燃烧时是一种致命的气体。
二氧化硫
化学式 SO 2的化合物是二氧化硫。它是一种有毒气体,会引起火柴烧焦的气味。它是由火山活动自然排放的,是铜提取和含硫化石燃料燃烧的副产品。二氧化硫具有类似硝酸的强烈气味。
SO 2的结构和键合
SO 2是弯曲的分子。仅考虑 s 和 p 轨道的价键理论方法将键合解释为两个共振结构之间的共振。硫-氧键的键阶为 1.5。这种不需要轨道合作的简单技术得到了支持。根据电子计数形式,硫原子具有+4的氧化态和+1的形式电荷。

二氧化硫结构式
SO 2的发生
二氧化硫在地球上的浓度极低,在大气中的浓度约为 1 ppm。它可以在其他行星上以不同的浓度被发现,最值得注意的是金星的大气层,它是第三丰富的大气气体,浓度为 150 ppm。它与水结合产生硫酸云,这是地球全球大气硫循环的重要组成部分,并导致全球变暖。它被认为在伽利略卫星上以冰的形式大量出现——作为木卫一尾随半球的升华冰或霜,以及木卫二、木卫三和卡利斯托的地壳和地幔中,甚至可能以液体形式并与水迅速相互作用。
SO 2的制备
- 在实验室中,二氧化硫是通过金属亚硫酸盐或金属亚硫酸氢盐与稀酸反应制成的。例如,在稀硫酸和亚硫酸钠之间的反应中会产生它。
Na 2 SO 3 + H 2 SO 4 → Na 2 SO 4 + H 2 O + SO 2
- 它是商业上作为硫化矿石焙烧的副产品获得的。产生的气体被干燥、液化并储存在钢瓶中。
4FeS 2 (s) + 11O 2 (g) →2Fe 2 O 3 (s) + 8SO 2 (g)
SO 2的性质
- 它是一种无色气体,带有腐烂鸡蛋的气味。它极易溶于水。
- 它很容易液化。
- 它溶于水生成亚硫酸,使其具有酸味。
- 它既不可燃也不利于燃烧。
- 它是一种强氧化剂。
- 它也是一种还原剂。它还充当还原剂。
SO 2的用途
- 作为食品工业中的食品防腐剂。
- 它既可用作漂白剂,又可用作消毒剂以消除多余的氯。
- 在实验室中,它被用作试剂和溶剂。
- 尽管二氧化硫主要用于生产硫酸、三氧化硫和亚硫酸盐。
- 它还用作消毒剂、制冷剂、还原剂、漂白剂和食品防腐剂,特别是在干果中。
- 二氧化硫被用作消毒剂、制冷剂、还原剂、漂白剂和食品防腐剂,尤其是在干果中,尽管它主要用于生产硫酸、三氧化硫和亚硫酸盐。
Sulphur dioxide in the air
The burning of fossil fuels by power plants and other industrial facilities is the major source in the atmosphere. Smaller sources of emissions include industrial activities such as mineral extraction, natural sources such as volcanoes, and locomotives, ships, and other vehicles and heavy equipment that run on sulfur-rich gasoline.
二氧化硫的健康影响
- 短期接触二氧化硫会影响人体呼吸系统并使呼吸困难。哮喘患者,尤其是青少年,特别容易受到二氧化硫的影响。
- 导致空气中高 SO 2浓度的二氧化硫排放通常会导致其他硫氧化物 (SO x ) 的产生。当 SO x与环境中的其他物质发生反应时,会产生小颗粒。
- 颗粒物 (PM) 污染是由这些颗粒引起的。小颗粒可以深入肺部,如果大量存在,可能会引起健康问题。
- 高浓度的气态 SO x会破坏树叶和减缓生长,从而伤害树木和植物。由 SO2 和其他硫氧化物引起的酸雨会破坏脆弱的生态系统。
示例问题
问题一:二氧化硫的性质是什么?
回答:
Sulfur dioxide is an acidic gas, which may be easily proved by filling a gas container with water and a few drops of universal indicator. Sulphurous acid is formed, which is a slightly dibasic acid.
问题二:二氧化硫是如何形成酸雨的?
回答:
Sulphur dioxide and nitrogen oxides are released into the atmosphere and carried by wind and air currents, resulting in acid rain. Sulfuric and nitric acids are formed when both oxides react with water, oxygen, and other molecules. They are then mixed with water and other seasonings before being served.
问题三:什么是酸雨?
回答:
Rain or any other form of precipitation that is highly acidic, suggesting that it includes significant levels of hydrogen ions, is referred to as acid rain. The pH of most water, including the water we drink, is between 6.5 and 8.5, but acid rain has a pH lower than this.
问题4:一氧化硫是如何形成的?
回答:
An electric discharge produces an unstable colourless gas in a low-pressure combination of sulphur dioxide and sulphur vapour; upon cooling, it condenses to an orange-red solid that slowly decomposes to sulphur and sulphur dioxide.
问题5:二氧化硫的结构是什么?
回答:
Sulfur dioxide is a bent molecule. A valence bond theory method that only considers s and p orbitals would explain the bonding as resonance between two resonance structures.
问题6:二氧化硫是如何形成的?
回答:
Sulfur dioxide is produced through the combustion of fossil fuels (coal and oil) and the smelting of sulphur-containing mineral ores (for example, aluminium, copper, zinc, iron and lead). Sulfur dioxide molecules easily dissolve in water to form sulfuric acid.
问题7:二氧化硫是化合物吗?
回答:
Sulfur dioxide is a hazardous inorganic gas that is thick and colourless. It can be created in large amounts during the intermediary processes of producing sulfuric acid. Sulfur dioxide also has a distinct and unpleasant odour that is akin to the aroma of a freshly struck match.