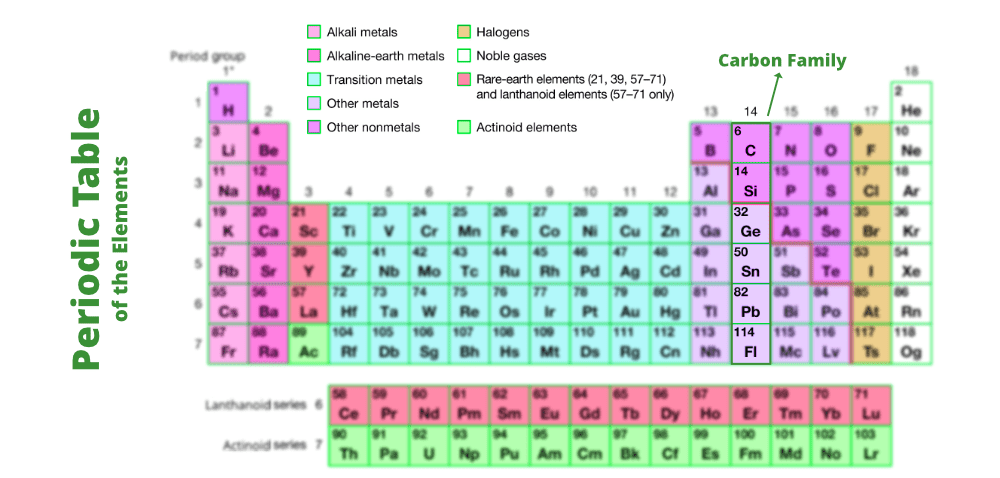
第 14 组元素:碳族
由于一个 p 亚壳具有三个简并 p 轨道,每个轨道可以容纳两个电子,因此总共有六组 p 块元素。由于它们倾向于失去一个电子,它们是有光泽的并且通常是电和热的良好导体。镓是一种可以在我们手中熔化的金属。硅是玻璃的重要组成部分,也是p-block组中最重要的准金属之一。
The last electron in a p-block element enters one of the three p-orbitals of its respective shell.
第 14 组元素——碳族
第 14 组元素是元素周期表 p 块中的第二组。它也被称为碳基团。碳 (C)、硅 (Si)、锗 (Ge)、锡 (Sn)、铅 (Pb) 和 Flerovium (Fl) 是该组的成员。
电子配置
The general electronic configuration of the group 14 elements is ns2 np2.
这些元素的最外层 p 轨道包含两个电子。因为第 14 族中的所有元素在它们的最外层都有四个电子,所以它们的化合价是四。他们使用这些电子形成键来实现八位组配置。
氧化态和惰性对效应
The general oxidation states of group 14 elements are +4, and +2. The tendency to form +2 ions increases as we move down the group. This is because of the inert pair effect. P-block elements exhibit this effect. This is explained by the inert pair effect. It is the absence of the s-orbital during bonding due to insufficient shielding of the intervening electrons.
电子填充 Sn 和 Pb 等元素的 d 和 f 轨道。由于 d 和 f 轨道的屏蔽能力较差,因此渗出的核电荷将 s 轨道吸引到更靠近原子核的位置。结果,s-轨道不愿意键合,只有p电子参与键合。结果,Pb +4是一种极好的氧化剂。
Anomalous Behaviour of Carbon
Carbon differs from the other elements in the group due to its small size, high electronegativity, high ionization enthalpy, and lack of d-orbital in the Valance Shell.
第 14 族元素的化学性质
- 共价半径:第 14 族元素的半径小于第 13 族元素的半径。有效核电荷的增加可以解释这一点。半径从 C 到 Si 的增加是显着的,其次是半径增加较小。这是由于 d 和 f 轨道的屏蔽不良,这增加了有效核电荷,导致半径变小。
- 电离焓:第 14 族元素的电离能高于第 13 族元素。这可以归因于物理尺寸。电离焓随着组的向下移动而降低。从 C 到 Si,有一个急剧下降,然后是名义上的下降。顺序如下: C > Si > Ge > Pb > Sn。由于 d 和 f 轨道的屏蔽无效,在这种情况下,Pb 具有比 Sn 更高的电离焓。
- 电负性:由于尺寸小,该族元素的电负性略高于第 13 族元素。从 Si 到 Pb 的元素的电负性值几乎相同。
第 14 族元素的物理性质
- 金属字符:由于 由于它们的小尺寸和高电离焓,第 14 族元素的正电性低于第 13 族元素。随着您在该族中前进,金属字符会变得更强。 Sn和Pb是低熔点的软金属,而C和Si是非金属,Ge是准金属。
- 熔点和沸点:碳、硅和锗因其极其稳定的固体结构而具有极高的熔点和沸点。由于惰性对效应,Sn 和 Pb 的熔点较低,因为只形成了两个键而不是四个键。碳的熔点非常高。第 14 族中的所有元素都具有类金刚石晶格结构,在自然界中极为稳定。这些高度稳定的晶格结构由于熔化过程而被破坏。随着原子大小的增加,熔点随着 MM 键的减少而降低。因为锡和铅是金属,它们的熔点显着降低。
- 四种共价化合物:四种共价化合物是价壳中的四个电子积极参与键合的化合物。第 14 组中的大多数元素都具有此属性。
- 密度:密度随着原子序数的增加而增加,这是由于基团下每单位体积的质量增加。
Some important Compounds formed by Group 14 Elements
Oxides of Group 14
MO and MO2 oxides are formed by group 14 elements. Lead can also form the oxide Pb3O4, which is a mixture of PbO and PbO2. CO is a neutral monoxide, GeO is basic, and SnO and PbO are amphoteric. C is sp hybridized in CO2. It differs from SiO2, which is sp3 hybridized Si. Each O atom in SiO2 is bonded to two Si bonds. As a result, SiO2 has a three-dimensional structure. This also attests to its high melting point. The acidic character of the dioxides decreases as one moves down the group.
Halides of Group 14
They combine to form MX4 tetrahalides. The central atom has been sp3 hybridized and has taken on a tetrahedral shape. Elements below carbon have empty d-orbitals, which allow them to back the bond with halogens. Dihalides are not formed by carbon. The dihalides have a bent shape and are sp2 hybridized.
对水的反应性:水对碳、硅或锗没有影响。锡与蒸汽反应生成二氧化 碳和氢气。水对铅没有影响,很可能是由于形成了保护性氧化膜。
碳族氧化物的用途
- 一氧化碳
- 一氧化碳是一种非常重要的工业气体,因为它用于生产许多有机和无机化合物。
- 它用于在气调包装系统中保持包装肉类的新鲜。
- 在高功率红外激光器中,它被用作激光介质。
- 二氧化碳
- 二氧化碳用于各种行业,包括石油、食品和化学工业。
- 它用于各种化学工业的尿素生产。
- 在食品工业中用作食品添加剂。
- 这是一种在灭火器中发现的化学物质。
- 二氧化硅
- 二氧化硅主要用于制造玻璃,用于窗户、瓶子和其他应用。
- 它是砂型铸造中的关键部件,负责生产各种工程部件和其他材料。
- 是食品工业中常用的添加剂。
- 有机硅
- 在汽车工业中,它被用作润滑剂。
- 在二氧化硅基基材的涂层中,使用有机硅。
- 由于其良好的铺展性和低水溶性,它被用作消泡剂中的活性化合物。
示例问题
问题 1:什么是 p 块元素?
回答:
The p-block is a region of the periodic table that includes columns IIIA to VIIIA but excludes helium. There are 35 p-block elements, each with valence electrons in the p orbital. The p-block elements are a diverse group of elements with a wide range of properties.
问题 2:为什么它们被称为 p 块元素?
回答:
Their name comes from the fact that their valence electrons are in the p orbital. To distinguish them from the transformation sequence and internal transformation, these are frequently referred to as Standard Components.
问题3:什么是连锁?
回答:
Catenation is the ability of an element to form covalent bonds with other atoms of the same element, resulting in the formation of an atom chain.
问题 4:第 14 组中的哪个元素表现出连锁?
回答:
To a large extent, carbon exhibits the catenation property. Carbon atoms, for example, can combine to form long chains, branched chains, and closed rings.
问题 5:为什么碳的行为与其他 14 族元素不同?
回答:
Carbon differs from the other elements in the group due to its small size, high electronegativity, high ionization enthalpy, and lack of d-orbital in the Valance Shell.