配位化合物的异构现象
过渡金属结合形成大量复杂的化合物,其中金属原子通过电子共享与许多阴离子或中性分子结合。在现代语言中,这种化合物被称为配位化合物。配位化合物的化学在现代无机化学中非常重要。叶绿素、血红蛋白和维生素 B12 分别是镁、铁和钴的配位化合物。配位化合物用于各种冶金工艺、工业催化剂和分析试剂。配位化合物还广泛用于电镀、纺织染色和药物化学。
配位化合物的一些例子是:
- 四羰基镍 (0) – [Ni(CO) 4 ]
- 四羟基锌酸钾 (II) – K 2 [Zn(OH) 4 ]
- 五氨合碳合钴 (III) 氯化物 – [Co(NH 3 ) 5 (CO 3 )]Cl
- 二胺氯硝基-N-铂(II) – [Pt(NH 3 ) 2 Cl(NO 2 )]
配位化合物的异构现象
Isomers are two or more compounds with the same chemical formula but a different atomic arrangement. They differ in one or more physical or chemical properties due to the different arrangements of atoms. Among coordination compounds, there are two major types of isomerism.
- Stereoisomerism
- Structural isomerism
立体异构
立体异构体具有相同的化学式和化学键,但它们的空间排列不同。
- 几何异构
由于配体的各种几何排列,这种类型的异构现象发生在杂配配合物中。坐标编号 4 和 6 提供了这种行为的显着示例。式[MX 2 L 2 ]的正方形平面配合物中的两个配体X(X和L是单齿的)可以以顺式异构体彼此相邻或以反式异构体彼此相对排列。
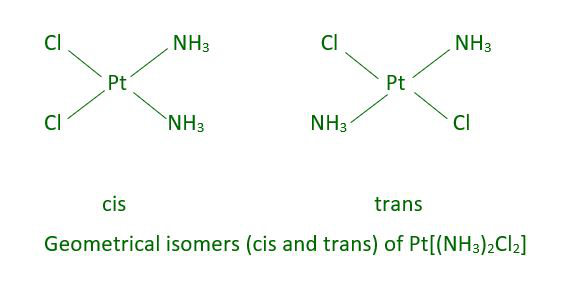
MABXL 类型的其他方形平面配合物(其中 M 是金属,A、B、X、L 是未鉴定的配体)表现出三种异构体——两种顺式和一种反式。这种异构现象对于四面体几何形状是不可能的,但在式[MX 2 L 4 ] ] 的八面体配合物中可能有类似的行为,其中两个配体X可以彼此顺式或反式取向。

当双齿配体 L – L [例如,NH 2 CH 2 CH 2 NH 2 (en)] 存在于分子式 [MX 2 (L– L) 2 ] 的配合物中时,这种类型的异构现象也称为几何异构现象。
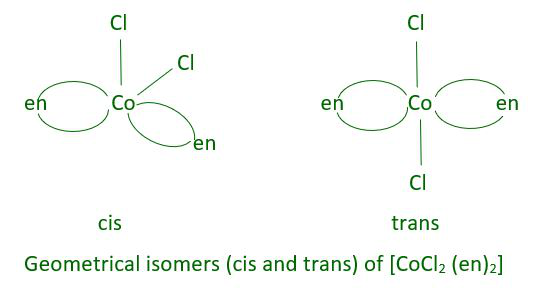
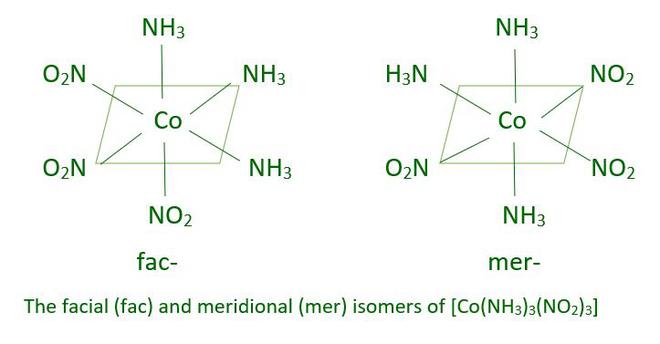
另一种类型的几何异构现象出现在[Ma 3 b 3 ] 类型的八面体配位实体中,例如[Co(NH 3 ) 3 (NO 2 ) 3 ]。当同一配体的三个供体原子占据八面体面角的相邻位置时,形成面(fac)异构体。当位置以八面体的子午线为中心时,获得经向(mer)异构体。
- 光学异构:
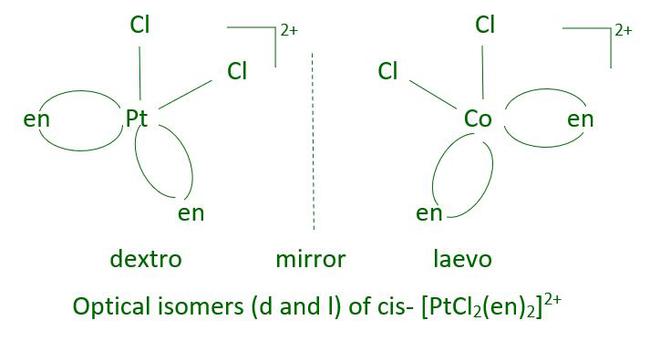
不能相互叠加的镜像是光学异构体。这些被称为对映异构体。手性分子或离子是那些不能叠加的分子或离子。这两种形式被称为 dextro (d) 和 laevo (l),具体取决于它们在旋光计中旋转偏振光平面的方向(d 向右旋转,l 向左旋转)。在含有双齿配体的八面体配合物中,光学异构现象很常见。

在[PtCl 2 (en) 2 ] 2+类型的配位实体中,只有顺式异构体显示出旋光活性。
结构异构
- 连锁异构:
在含有二元配体的配位化合物中,会发生连接异构现象。含有硫氰酸盐配体 NCS- 的配合物提供了一个简单的例子,因为它可以通过氮结合产生 M-NCS 或通过硫结合产生 M-SCN。这种行为表现在络合物 [Co(NH 3 ) 5 (NO 2 )]Cl 2中,它以红色形式获得,其中亚硝酸盐配体通过氧 (-ONO) 结合,黄色形式,其中亚硝酸盐配体通过氮(-NO 2 )结合。
Examples:
- violet-colored [(NH3)5Co-SCN]2+ and orange-colored [(NH3)5Co-NCS]2+
- [Co(ONO)(NH3)5]Cl : the nitrito isomer -O attached and [Co(NO2)(NH3)5]Cl : the nitro isomer – N attached
- 配位异构:
复合物中存在的不同金属离子的阳离子和阴离子实体之间的配体交换导致配位异构。 [Co(NH 3 ) 6 ][Cr(CN) 6 ] 提供了一个例子,其中 NH3 配体与 Co 3+结合,CN- 配体与 Cr 3+结合。在其配位异构体[Cr(NH 3 ) 6 ][Co(CN) 6 ]中,NH 3配体与Cr 3+结合,CN -配体与Co 3+结合。
Examples:
- [Co(NH3)6][Cr(C2O4)3 ] and [Co(C2O4)3][Cr(NH3)6]
- [Zn(NH3)4][Cu(Cl4)] and [Cu(NH3)4][Zn(Cl4)]
- 电离异构:
当复合盐中的反离子本身是潜在的配体并且可以取代配体,然后配体可以成为反离子时,就会发生电离异构现象。电离异构体 [Co(NH 3 ) 5 (SO 4 )]Br 和 [Co(NH 3 ) 5 Br]SO4 提供了一个例子。
Examples:
- [Co(NH3)5Cl]SO4 and [Co(NH3)5(SO4)]Cl
- [CoBr(H2O)5]+Cl– and [CoCl(H2O)5]+Br–
- 溶剂化物异构:
溶剂化物异构体被称为“水合物异构体”,在这种异构体中,水作为溶剂涉及。这类似于电离异构。硫酸盐异构体之间的区别在于溶剂分子是直接与金属离子键合还是作为游离溶剂分子存在于晶格中。水络合物 [Cr(H 2 O) 6 ]Cl 3 (紫色)及其溶剂化物异构体 [Cr(H 2 O) 5 Cl]Cl 2 .H 2 O 就是两个例子(灰绿色)。
Examples:
- [CrCl2(H2O)4]Cl.2H2O : bright-green colored
- [CrCl(H2O)5]Cl2.H2O: grey-green colored
- [Cr(H2O)6]Cl3: violet colored
已解决的问题:
问题 1:画出 [Fe(NH 3 ) 2 (CN) 4 ] –的所有几何异构体。
回答:
问题 2:指出下列配合物的异构类型
- [Co(en) 3 ]Cl 3
- [Co(NH 3 ) 5 (NO 2 )](NO 3 ) 2
- [Pt(NH 3 )(H 2 O)Cl 2 ]
回答:
- [Co(en)3 ]Cl3 —-> Optical isomerism
- [Co(NH3 )5 (NO2 )](NO3 )2 —-> Optical isomerism, Linkage isomerism, Ionization isomerism
- [Pt(NH3 )(H2O)Cl2 ] —-> Geometrical (cis-, trans-) isomerism
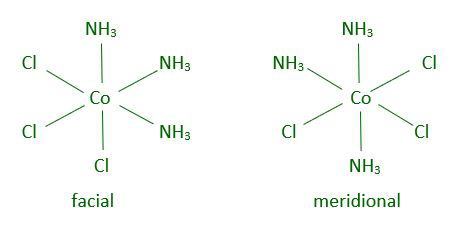
问题 3:[Co(NH 3 ) 3 (Cl) 3 ] 中可能有多少几何异构体?
回答:
Two geometrical isomer is possible for [Co(NH3)3(Cl)3]–
问题4:配位化合物中的配体是什么?
回答:
Ligands are ions or molecules that are bound to the central atom/ion of the coordination entity. Simple ions like Cl–, small molecules like H2O or NH3, larger molecules like H2NCH2CH2NH2 or N(CH2CH2NH2)3 , and even macromolecules like proteins can fall into this category.
问题 5:画出 [Pt(NH 3 )(Br)(Cl)(py)] 的几何异构体?
回答:

