与配位化合物有关的重要术语
配位化合物由中心金属原子或离子组成,中心金属原子或离子被许多带相反电荷的离子或中性分子包围。配位化合物中的所有离子或分子都通过配位键与中心金属原子相连。当配位化合物溶解在水中时,它们不会解离成简单的离子,这意味着它在水中不会失去其身份。配位化合物也称为配位化合物。配位化合物在我们的日常生活中非常重要。重要的是要认识到植物中的叶绿素(Mg-复合物)、人体血液中的血红蛋白(Fe-复合物)和维生素 B12(Co-复合物)也是复合物。
配位化合物中相关术语的定义:
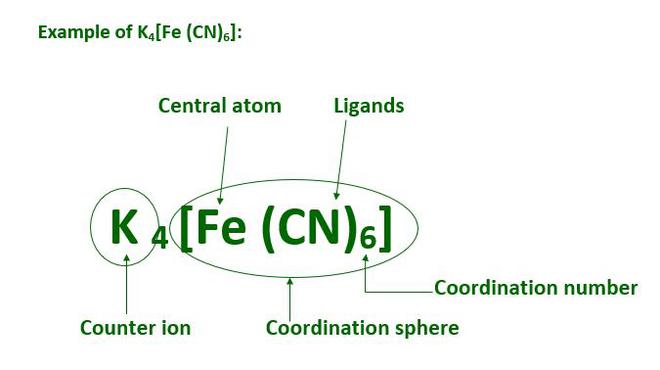
协调单位:
配位实体由与一定数量的离子或分子键合的中心金属原子或离子组成。这里[CoCl 3 (NH 3 ) 3 ]是具有三个氯离子和三个与钴离子相连的氨分子的配位实体。
一些重要的例子是:
- [Ni(CO) 4 ],
- [PtCl 2 (NH 3 ) 2 ],
- [Fe(CN) 6 ] 4– , 和
- [Co(NH 3 ) 6 ] 3+
中心原子/离子:
中心原子被一个或多个以特定几何排列的中性分子或离子包围并配位键合,并以配位键连接。配位体[NiCl 2 (H 2 O) 4 ]、[CoCl(NH 3 ) 5 ] 2+和[Fe(CN) 6 ] 3–中的中心原子/离子是Ni 2+ 、Co 3+ 、和 Fe 3+ ,分别。
一些重要的例子是:
- K 4 [Fe(CN) 6 ] – 中心原子/离子是 : Fe +2
- [Cu(NH 3 ) 4 ]SO 4 – 中心原子/离子为:Cu +2
配体:
配体是简单的离子或分子,具有提供电子的倾向,可以与中心原子/离子形成配位键。配体可以是简单的离子如 Cl– 和 Br – ,小分子如 H 2 O 或 NH 3 ,大分子如 H 2 NCH 2 CH 2 NH 2或 N(CH 2 CH 2 NH 2 ) 3 。
当配体通过单个供体原子与金属离子结合时,则称该配体是单齿的。 Cl – 、H 2 O 或 NH 3是单齿配体。当配体通过两个供体原子连接时,称该配体是双齿的。 H 2 NCH 2 CH 2 NH 2 (ethane-1,2-diamine) 或 C 2 O 4 2- (oxalate) 是二齿配体。当单个配体中存在多个供体原子时,例如 N(CH 2 CH 2 NH 2 ) 3 ,该配体称为多齿配体。乙二胺四乙酸根离子(EDTA 4- )是一种非常重要的六齿配体。它可以通过两个氮原子和四个氧原子连接到一个中心金属离子。
二元配体是具有两个不同的供体原子并且可以是复合物中的两个配体中的任一个的配体。 NO 2–和 SCN –离子是此类配体的两个例子。 NO 2–离子可以通过氮或氧与中心金属原子/离子配位。同样,SCN –离子可以通过硫原子或氮原子配位。

一些重要的例子是:
- 单齿配体:
- 氯——
- NH 3
- 双齿配体:
- H 2 NCH 2 CH 2 NH 2
- C 2 O 4 2–
协调号:
络合物中金属离子的配位数 (CN) 定义为与金属直接键合的配体供体原子的数量。例如,络离子[PtCl 6 ] 2-和[Ni(NH 3 ) 4 ] 2+中Pt和Ni的配位数分别为6和4。类似地,Fe 和 Co 在络合物离子 [Fe(C 2 O 4 ) 3 ] 3-和 [Co(en) 3 ] 3+中的配位数为 6,因为 C 2 O 4 2-和 en (ethane- 1,2-二胺)是二齿配体。
需要注意的是,中心原子/离子的配位数仅由配体与中心原子/离子形成的σ键数决定。该计算不包括配体和中心原子/离子之间形成的 pi 键。
一些重要的例子是:
- K 4 [Fe(CN) 6 ] – 配位数 = 6
- [Ni(CO) 4 ] – 配位数 = 4
协调范围:
配位球由中心原子/离子和与其相连的配体组成。可电离基团用括号表示,称为抗衡离子。
一些重要的例子是:
在配合物K 4 [Fe(CN) 6 ]中:配位球为[Fe(CN) 6 ] 4- ,反离子为K+。
协调多面体:
配位多面体由直接连接到中心原子/离子的配体原子的空间排列定义。八面体、正方形平面和四面体多面体是最常见的配位多面体。
一些重要的例子是:
- [Co(NH 3 ) 6 ] 3+是八面体,
- [Ni(CO) 4 ] 是四面体,并且
- [PtCl 4 ] 2–是正方形平面。
中心原子的氧化数:
配合物中中心原子的氧化数定义为如果与中心原子共享的所有配体和电子对都被去除,它将携带的电荷。氧化数由配位实体名称后括号中的罗马数字表示。
一些重要的例子是:
- [Cu(CN) 4 ] 3-中铜的氧化数为+1,记作Cu(I)。
- K 4 [Fe(CN) 6 ]中亚铁的氧化数为+2,记作Fe(II)。
同配体和异配体配合物:
同配络合物是其中金属仅与一种类型的供体基团结合的那些,例如[Co(NH 3 ) 6 ] 3+。杂配络合物是其中金属与一种以上类型的供体基团结合的那些,例如[Co(NH 3 ) 4 Cl 2 ] + 。
一些重要的例子是:
- 同配络合物:
- K 2 [Zn(OH) 4 ]
- [Ni(CO) 4 ]
- 杂配体:
- [Co(NH 3 ) 4 (H 2 O)Cl]Cl 2
- [Pt(NH 3 ) 2 Cl(NO 2 )]
示例问题
问题 1:在下列化合物中写出中心原子/离子——
- K 2 [Zn(OH) 4 ]
- [Co(NH 3 ) 4 (H 2 O)Cl]Cl 2
- K 3 [Al(C 2 O 4 ) 3 ]
- [CoCl 2 (en) 2 ]+
- [Ni(CO) 4 ]
回答:
- Central atom of K2[Zn(OH)4] is – Zn
- Central atom of [Co(NH3 )4 (H2O)Cl]Cl2 is – Co
- Central atom of K3 [Al(C2O4 )3 ] is – Al
- Central atom of [Pt(NH3 )2Cl(NO2 )]+ is – Pt
- Central atom of [Ni(CO)4 ] is – Ni
问题2:写出下列配位化合物的配位数——
- K 4 [Fe(CN) 6 ]
- [Ni(CO) 4 ]
- K 3 [Al(C 2 O 4 ) 3 ]
回答:
- K4[Fe(CN)6] – coordination number = 6
- [Ni(CO)4 ] – coordination number = 4
- K3 [Al(C2O4 )3 ] – coordination number = 6
问题3:什么是双配体,举例说明?
回答:
A molecule or an ion that has two donor atoms but only one of them forms a coordinate bond with the central metal atom is referred to as a ambidentate ligands.
Some important examples are:
- CN–
- NC:–
- NO2-
- ONO:–
问题 4:写出下列配位化合物中存在的所有配体——
- [铂(NH 3 ) 6 ] 4+
- [Co(NH 3 ) 2 Cl 2 (en)] +
- [CO(NH 3 ) 5 NO 2 ] 2+
- [Cu(Br) 4 ] 2-
回答:
- Ligands in [Pt(NH3)6]4+ are : NH3
- Ligands in [Co(NH3)2Cl2(en)]+ are: NH3, Cl–, en
- Ligands in [CO(NH3)5NO2]2+ are: NH3, NO2-
- Ligands in [Cu(Br)4]2- are: Br–
问题 5:找出下列复杂化合物中金属的氧化数——
- Co(H 2 O)(CN)(en) 2 ] 2+
- [CoBr 2 (en) 2 ] +
- [PtCl 4 ] 2-
- K 3 [Fe(CN) 6 ]
- [Cr(NH 3 ) 3 CI 3 ]
回答:
1. Co(H2O)(CN)(en)2]2+
Oxidation number: x + 0 + (-1) + 0 = +2
x = +3
2. [CoBr2(en)2]+
Oxidation number: x + 2*(-1) + 0 = +1
x = +3
3. [PtCl4]2-
Oxidation number: x + (-4) = -2
x = +2
4. K3[Fe(CN)6]
Oxidation number: 3*(+1) + x + 6*(-1) = 0
x = +3
5. [Cr(NH3)3CI3]
Oxidation number: x + 0 + 3*(-1) = 0
x = +3