元素在周期表中的位置
元素周期表中间的元素,从第 3 族到第 12 族,被称为 d 区元素。 d-block 的名称来自于最后一个电子进入倒数第二个壳层的 d 轨道这一事实。这些通常被称为过渡元素,因为它们的性质介于高反应性金属 s-block 元素和非金属 p-block 元素之间。 d 块包含四个系列,对应于 3d、4d、5d 或 6d 轨道的填充。
一般而言,过渡元素是对应于现代元素周期表(第 3-12 族)的 d 区的任何元素。镧系元素和锕系元素是 f 区元素,也可以归类为过渡金属。然而,由于 f 区元素包含部分 f 轨道,它们也被称为内过渡元素或内过渡金属。
过渡元素的一般性质
电子构型对应于(n-1)d 5 ns 1或(n-1)d 10 ns 1 。这是由于半满或完全充满的电子轨道提供的稳定性。锌、镉和汞不被视为过渡元素,因为它们的电气配置不同于其他过渡金属。另一方面,其余 d 区元素的性质非常相似,这种相似性可以在元素周期表的每一行中看到。
当我们沿着元素周期表从左向右移动时,第二行和第三行元素的性质会逐渐变化。这些元素的外壳具有较差的屏蔽性能,随着更多的质子被添加到原子核中,这会提高有效核电荷。下面列出了过渡元素的特性。
- 当这些元素混合时,它们会形成五颜六色的化合物和离子。电子dd跃迁解释了它的颜色。
- 这些元素可能的氧化态之间的能量差异不大。因此,过渡元素具有广泛的氧化态。
- 由于 d 轨道中的不成对电子,这些元素会产生大量的顺磁性化合物。
- 各种各样的配体可以与这些元素结合。因此,过渡元素会产生多种稳定的复合物。
- 这些元素的电荷半径比非常高。
- 与其他元素相比,过渡金属较硬且密度相对较高。
- 由于离域 d 电子参与金属键合,因此这些元素具有高沸点和熔化温度。
- 由于离域d电子的金属键合,过渡元素也是良好的电导体。
在元素周期表中的位置:d 和 f – 块元素
研究哪些元素在元素周期表中的特定组位置对于整体理解这些元素很重要。元素周期表中的不同元素被分类是有原因的。 d 和 f 块组件具有使它们符合此类别的某些特征。
d-block 元素由填充壳 3d、4d 和 5d 的电子产生的元素组成。它们也被称为过渡元素,因为它们的元素周期表位置在 s-block 和 p-block 元素之间。它们的性质在 s 嵌段的极易反应的金属元素(通常形成离子化合物)和 p 嵌段的主要共价元素之间过渡。
D-嵌段元素或过渡元素是具有部分填充d亚壳的那些元素或离子或那些其中微分电子占据(n-1)d亚壳的那些元素。他们命名了过渡元素,因为它们的属性揭示了从左侧(s-block)元素到轻侧(p-block 元素)的过渡。有四个 d 系列,每个都以 (n-1)d 1 ns 2开头,范围从第 3 组到第 12 组(或第 IIIB 组到第 II B 组)。
在 d 块中,电子被添加到倒数第二个壳层,将其大小从 8 增加到 18。通常,过渡元素具有未完成的 d 能级。第 12 族(锌)具有 ad 10构型,并且由于 d 壳是完整的,这些元素的化合物是不寻常的并且与其他元素不同。元素分为三个完整的行,每行十个元素,以及不完整的第四行。 f块部分用于讨论未完成的第四系列的位置。这些元素包括贵金属,如银、金和铂,以及工业上重要的元素,如铁、铜和镍。
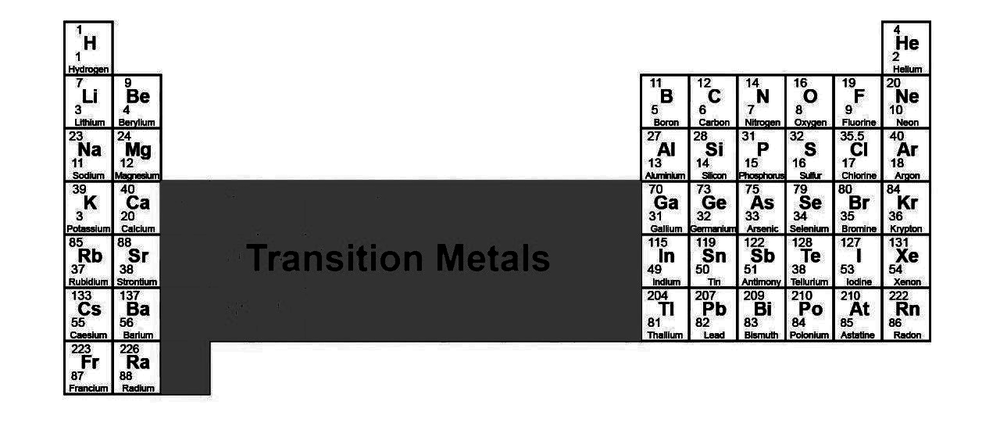
过渡金属在元素周期表中的位置
- 内部过渡元素是“f”的另一个术语——块元素。在这些元素中,最后一个电子通常进入轨道的倒数第二个,即 (n – 2) f。过渡元素中的区别电子可以进入 4f 或 5f 轨道,使它们可以进一步分类为镧系元素或锕系元素。
- 镧系元素中的微分电子到达4f轨道。这些范围从铈到镥。镧系元素以直接出现在镧之后的元素命名。锕系元素中的微分电子进入 5f 轨道。通常,它们是钍到铼。
- 在元素周期表中,这些元素紧随其后的锕。 (n–2) f 1–14 (n–1) d 0–1 ns2 是 f 块元素的一般电子配置。镧系元素的电子构型为 [Xe]4f 1-14 5d 0-1 6s 2 ,而锕系元素的电子构型为 [Rn]5f 1-14 6d 0-1 7s 2 。
示例问题
问题1:过渡金属的金属特性是什么?
回答:
Malleability, ductility, high tensile strength, and metallic lustre are all characteristics of transition metals. They are good heat and electrical conductors and have a tendency to crystallise. Trends in the metallic properties of transition elements, on the other hand, are visible. Elements such as chromium and molybdenum are among the hardest transition metals because they contain a large amount of unpaired electrons.
问题2:为什么所有的过渡元素都是金属?
回答:
All transition elements are metals because their outermost shells contain only two electrons. Because of the strong metallic linkages, they are also malleable, durable, and ductile.
问题 3:d-block 元素与 f-block 元素有何不同?
回答:
The last electron in the d-block enters the d-orbital of the penultimate shell. The electron enters the f-orbital of the anti-penultimate shell in the f-block elements. The oxidation state of d-block elements varies, whereas the oxidation state of most f-block elements is +3. Almost all d-blocks are stable, whereas a greater proportion of f-blocks are radioactive.
问题4:过渡元素的催化性能是什么?
回答:
Because of the presence of unoccupied d-orbitals, the tendency to exhibit fluctuating oxidation states, the ability to generate reaction intermediates with reactants, and the presence of defects in their crystal lattices, transition elements exhibit catalytic capabilities.
问题 5:为什么 d – 嵌段元素具有高熔点和沸点?
回答:
In addition to metallic bonding by s-electrons, unpaired electrons and vacant or partially full d-orbitals produce covalent bonds. D-block elements have higher melting and boiling temperatures than s and p block elements due to their strong bonding. This trend continues until the d5 configuration, at which point it begins to decline as more electrons are coupled in the d-orbital.