共价键——定义、类型、性质、例子
在旧式材料科学和普通科学中,物质被描述为任何具有质量和吞噬空间的物质。可以达到的逐步战斗最终包含原子,这些原子参与了亚原子粒子的协同工作,而物质意味着粒子和包括它们在内的一切,就像任何粒子一样,在这两种标准中,它们都具有静止质量和体积和连贯的使用。无论如何,加入像光子这样的无质量粒子,就像其他能量奇迹或像光一样的波。问题状态的范围很广。
各种状态,类似于等离子体、玻色-爱因斯坦凝聚态、费米子凝聚态和夸克-胶子等离子体,都是可能的,无论固体、液体和气体的常见时代如何——例如,水以冰、液态水和蒸气的形式存在蒸汽——但各种状态,例如等离子体、玻色-爱因斯坦凝聚态、费米子凝聚态和夸克-胶子等离子体,也是可能的。除此之外,它被分离成纯物质和混合物。
什么是化学键?
Chemical bonding is the process of joining two or more atoms that involves the redistribution of electrons such that each atom engaged in the bonding obtains a stable electronic state.
每一个 iotas 都通过获得最接近的受人尊敬的气体电子装置来完成他们的 duplet 或 octet 以实现安全性。它往往是通过发展粒子之间的复合连接来实现的。
iota可以通过三种方式形成物质键,
- 通过将至少一个电子丢失给另一个 iota。
- 通过从另一个 iota 获取至少一个电子。
- 通过将至少一个电子传递给另一个 iota
化学键的类型
化学键分为四类:
- Ionic键或电价键
- 共价键
- 氢键
- 极性共价键
共价键
- 简单来说,共价键是粒子之间的电子共享,以完成对单个 iotas 感兴趣的光荣气体设置。
- 共价键中的微量元素通过着迷的静电力结合在一起。这种力量位于增强粒子的明显带电核心和它们共享的带相反电荷的电子的中间。
- 以共价键连接 iotas 的电子称为保持电子对。这些保持电子对带来了称为原子的离散粒子集合的排列,这是具有该化合物合成字符的化合物的最小部分。
- 这种保持发生在偶然表中相似成分或彼此靠近的成分的两个粒子之间。这种持有主要发生在非金属之间;在任何情况下,同样可以在非金属和金属之间看到。
共价键的类型
共价键的排列产生了特定的键长。这种键长是混合物的商标属性,它解决了几种权力之间的和谐,例如,
- 带电的核心和带相反电的电子之间的吸引力,
- 两个带相反电荷的电子之间的排斥,和
- 两个明显带电的核心之间的排斥力。
更有限的键长具有更显着的键强度。鉴于键长,共价键属于伴随类型。
- 单共价键
- 双共价键
- 三重共价键
单共价键
A single covalent bond is framed by the common sharing of one electron pair between two molecules. In a single covalent bond, every particle contributes one electron for sharing. It is addressed by a solitary line (–) between the two iotas sharing electrons.
- 氯分子的形成:氯的价壳层有七个电子,它还需要一个电子来完成它的八位字节。结果,它可能与另一个氯原子共享一个电子,形成一个氯分子,如下图所示:
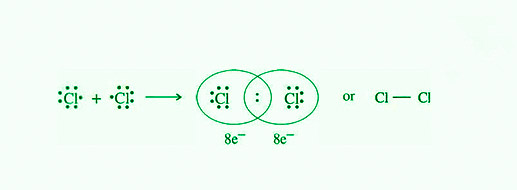
- 甲烷分子(CH 4 )的形成:碳原子的最外层有四个电子(价层)。它的价电子与四个 H 原子共享。结果,一个碳原子与四个氢原子产生了四个单独的共价连接。

甲烷分子以图形方式显示为:
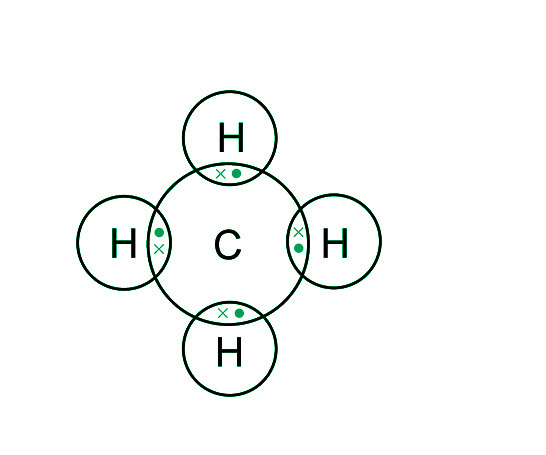
甲烷分子中的碳原子和四个氢原子中的每一个都采用氖和氦的稳定电态。甲烷中有四个碳氢(C-H)单键。因此,一个甲烷分子有四对共享的电子。
双共价键
The mutual sharing of two-electron pairs between two atoms forms a double covalent bond. Each atom offers two electrons for sharing in a double covalent connection. It symbolises the two atoms sharing electrons by a double line (=).
- 乙烯分子 (C 2 H 4 ) 的形成:两个 C 原子中的每一个都与两个 H 原子连接,在乙烯分子 (C 2 H 4 ) 的形成过程中形成两个单独的共价键。每个 C 原子的剩余两个电子在两个 C 原子之间形成一个双键。
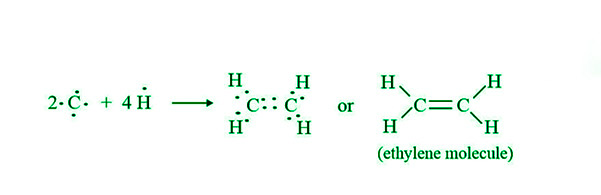
- 二氧化碳分子(CO 2 )的形成:碳的价层有四个电子,需要四个电子来完成它的八位字节,而氧的价壳有六个电子,需要两个电子才能完成它的八位字节。碳可以通过与两个氧原子共享两个电子对来形成两个双键来完成其八位字节。下图描述了二氧化碳 (CO 2 ) 分子的产生:
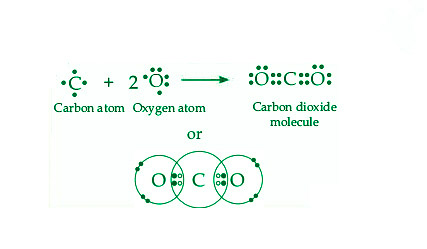
三重共价键
The mutual sharing of three electron pairs between two atoms forms a triple covalent connection. Each atom gives three electrons for sharing in a triple covalent connection. The two atoms sharing electrons are represented by a triple line (≡).
- 乙炔分子(C 2 H 2 )的形成:两个C原子与两个H原子结合形成乙炔分子。每个 C 原子的三个价电子与另一个 C 原子共享。结果,每个C原子的一个电子和一个H原子的一个电子被共享。
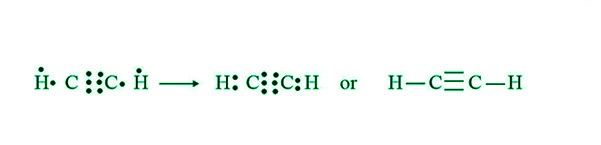
因此,乙炔分子中的两个 C 原子之间存在三重共价键,每个 C 原子通过单个共价键连接到一个 H 原子。因此,乙炔分子可以被视为:
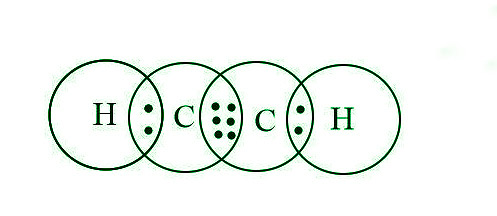
共价化合物的性质
- 物理状态:通常,共价混合物是流体或气体,因为它们的粒子之间具有微弱的共价吸引力。其中一些是固体。
- 溶解性:它们不溶于水,但可溶于天然溶剂。尽管如此,一些共价混合物,如糖、尿素、葡萄糖、碱、氯化氢等,可溶于水。
- 熔点和沸点:它们具有低软化点和沸腾边缘。它只需要一点点能量就可以打破共价混合物粒子之间微弱的共价魅力。
- 电导率:共价混合物不具有直接功率,因为它们不含颗粒。在任何情况下,共价混合物(如嗅盐、氯化氢)在水中分解时都会产生电力。原因是氯化氢与水发生综合反应,形成含有盐酸腐蚀性的颗粒。
示例问题
问题1:解释三键的形成?
回答:
Nitrogen is a diatomic chemical that belongs to the VA family on the periodic table. With five valence electrons, nitrogen requires three additional valence electrons to complete its octet.
A nitrogen atom can fill its octet by sharing three electrons with another nitrogen atom, producing three covalent connections, the so-called triple bond.
问题2:什么是三价共价键?
回答:
The mutual sharing of three electron pairs between two atoms forms a triple covalent connection. Each atom gives three electrons for sharing in a triple covalent connection. The two atoms sharing electrons are represented by a triple line (≡).
问题3:什么是共价键?
回答:
A covalent bond is a chemical connection established between two atoms as a result of the mutual sharing of electrons. This is because the atoms only share their outermost electron, resulting in each atom having the inert gas’s stable electron configuration. Its covalency is the number of electrons shared between the atoms.
问题4:什么是化学键?
回答:
Chemical bonding is the process of joining two or more atoms that involves the redistribution of electrons such that each atom engaged in the bonding obtains a stable electronic state.
问题5:什么是双共价键?
回答:
The mutual sharing of two electron pairs between two atoms forms a double covalent bond. Each atom offers two electrons for sharing in a double covalent connection. It symbolises the two atoms sharing electrons by a double line (=).