卤素的含氧酸 – 定义、性质、结构
第 17 族元素从上到下依次为氟、氯、溴、碘和砹。它们被称为卤素,因为它们会产生盐。这个小组的成员彼此非常相似。它们具有一致的物理和化学特征模式。这些元素中的每一个的价壳都包含七个电子。他们的电子设置是 ns 2 np 5 。
如果酸中含有氧(称为含氧酸),则再次使用后缀 –ous 和 –ic 来表示酸式中氧的数量较少和较多。含氧酸由氢、氧和其他元素组成。含有氢、氧和其他元素的酸称为含氧酸。
第 17 组元素:卤素家族
第 17 组是第六个 p 区元素组。卤素一词源自希腊语 Halo 和基因。卤素源自单词 halo,意思是盐,和基因,意思是出生,所以卤素意味着盐生产者。当与碱金属或碱土金属相互作用时,第 17 族中的所有元素都会生成盐。因此,该族也称为卤素族,该族中的元素称为卤素。
卤素的含氧酸
氟、氯、溴、碘和砹都是第17族的成员。它们统称为卤素,意为制盐剂。这个小组的成员惊人地相似。随着我们在该组中的进展,物理和化学性质具有一致的渐变。我们不能以纯粹的形式将它们分开。在水溶液中,它们是稳定的。它们在盐形式中也非常稳定。次卤酸(+1氧化态)、亚卤酸(+3氧化态)、卤酸(+5氧化态)和高卤酸(+7氧化态)是卤素产生的四种含氧酸。
砹是该组唯一的放射性元素。它们的价层有七个电子(ns 2 np 5 ),比下一个惰性气体配置少一个。由于其有效的核电荷,卤素的大小适中。因此,它们不太可能失去电子,而更有可能获得电子来完成它们的八位字节。几种含氧酸是由卤素形成的(它们是酸性基团中含有氧的酸)。
卤素含氧酸的性质
- 氟非常小,具有很高的电负性。因此,它仅产生一种含氧酸 HOF,也称为氟 (I) 酸或次氟酸。卤素家族的其他成员结合起来产生许多含氧酸。它们不能以纯粹的形式被隔离。它们在水溶液中或作为盐是稳定的。
- 一般来说,卤素会产生四种类型的含氧酸:次卤酸(+1 氧化态)、亚卤酸(+3 氧化态)、卤酸(+5 氧化态)和高卤酸(+7 氧化态)。
- 氯可分解为四种类型的含氧酸。即,HOCl(次氯酸)、HOClO(亚氯酸)、HOClO 2 (氯酸)和HOClO 3 (次氯酸)(高氯酸)。
- 溴产生HOBr(次溴酸)、HOBrO 2 (溴酸)和HOBrO 3 (次溴酸)(高溴酸)。碘分解成HOI(次碘酸)、HOIO 2 (碘酸)和HOIO 3 (次碘酸)(高碘酸)。
卤素的含氧酸的结构
核心卤素原子在所有含氧酸中都是 sp3 杂化的。每个含氧酸至少包含一个 X-OH 键。 “X=O”键存在于大多数含氧酸中。在自然界中,含氧酸中中心卤素原子和氧之间的双键是 d pi - p pi。次氟酸、次氯酸、次溴酸和次碘酸是次卤酸的例子。在次卤酸中,卤素的氧化态为+1。由于中心卤素原子上存在三个孤对电子,次卤酸盐离子具有线性形式。
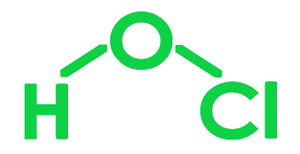
次氯酸
因为次卤酸不太稳定,它们往往会产生卤酸。
3HOX → HOXO 2 + 3HX
只有氟含氧酸是次氟酸。由于氟原子中没有 d 轨道,因此不知道氟的更高含氧酸。亚卤酸中仅包括亚氯酸。亚氯酸中氯的氧化态为+3。由于核心氯原子上存在两个孤对电子,亚氯酸盐离子呈V形。氯酸、溴酸和碘酸是卤酸的例子。在这些含氧酸中,卤素的氧化态为+5。由于中心卤素原子上存在孤对电子,因此盐酸盐离子具有锥体结构。

亚氯酸
高氯酸、高溴酸和高碘酸是高卤酸的例子。这些含氧酸的卤素氧化态为+7。过卤酸盐离子具有四面体结构。任何卤素含氧酸序列的第一个成员都具有高酸性。这是因为卤素具有很强的电负性并且尺寸很小。
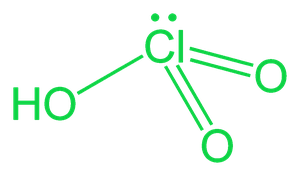
氯酸
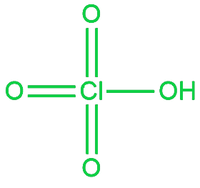
高氯酸
例如,高氯酸在高卤酸中具有很高的酸性。因为氯比溴或碘的电负性更大,所以 Cl-O 键中的共享电子对比 Br-O 键中的溴或 IO 键中的碘更接近氯。结果,在高氯酸的情况下,OH键变得非常弱,使得质子容易释放。含氧酸的酸强度随着卤素氧化数的增加而增加。
卤间化合物
卤素间化合物是由两种不同卤素反应产生的化合物。它们具有XX'、XX 3 '、XX 5 '和XX 7 '的一般组成,其中X是较大的卤素,X'是较小的卤素,并且X比X'更具正电性。随着 X 和 X' 的半径比增加,每个分子的原子数也增加。
示例问题
问题一:卤素的用途是什么?
回答:
The following are some of the most prevalent applications for halogens:
- Fluorine compounds are commonly found in toothpaste and drinking water supplies. Fluorine is a very important drug because it is strongly reactive with tooth enamel and delays tooth decay.
- Chlorine is widely utilised in the bleaching process. It is also used in the metallurgy of gold and platinum.
- Chlorine is a chemical that is used to purify drinking water.
- Iodine is an antiseptic and a good germicide.
问题2:什么是卤间化合物?
回答:
When halogens react with one another, interhalogen compounds are created. Their features and behaviours are midway between those of two-parent halogens. However, some features may differ. Except for IF7, all interhalogens can be created by mixing pure halogens under specific conditions.
问题 3:卤素的氧化态是什么?
回答:
The elements of the halogen family all have a -1 oxidation state. Fluorine, the most electronegative element, has only a -1 oxidation state. Elements with +1, +3, +5, and +7 states include chlorine, bromine, and iodine.
问题4:卤素如何与氧气反应?
回答:
When halogens react with oxygen, oxides are generated. However, it has been discovered that the oxides are unstable. In addition to oxides, halogens form a range of halogen oxoacids and oxoanions.
问题 5:卤素是良好的氧化剂吗?
回答:
The halogens are all excellent oxidizers. Fluorine is the most potent oxidizer on the list. It is capable of converting all halide particles to halogen.