炔烃——定义、结构、制备、性质
碳氢化合物是有机化学中完全由氢和碳组成的有机分子。碳氢化合物是第 14 组氢化物的一个例子。碳氢化合物是无色的、疏水的,并且只有微弱的气味。由于它们的分子结构不同,因此无法进一步概括。化石燃料的燃烧,包括燃料生产和燃烧,占人为碳氢化合物排放的大部分。植物的排放物是乙烯、异戊二烯和单萜等碳氢化合物的天然供应。
炔烃
In natural science, alkynes are the unsaturated hydrocarbons having something like a triple connection between carbon-carbon particles (– C≡C–). The overall recipe of this unsaturated hydrocarbon is CnH2n–2, where n–2, 3, 4, 5… .
Alkynes are customarily known as acetyls. Like different hydrocarbons, alkynes are additionally hydrophobic.
碳氢化合物是最简单的有机化合物,只有碳和氢作为成分。这些可以在自然界中以我们每天使用的物体的形式出现。因此,碳氢化合物被认为是有机化合物的母体。另一方面,所有其他化合物被认为是通过用官能团取代一个或多个氢原子而制成的。
炔烃的结构
碳-碳三键由一个数量为σ键和两个弱π键组成。
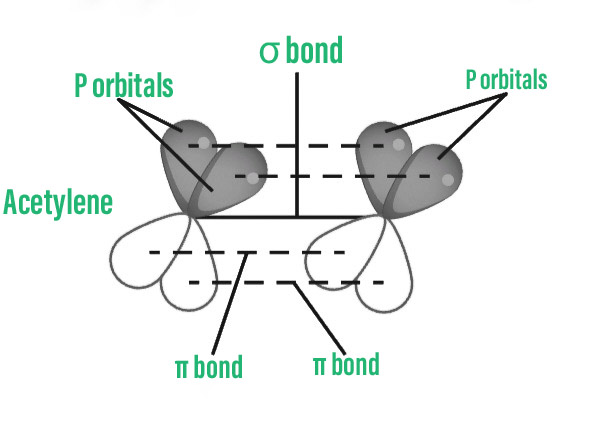
炔烃的结构
炔烃的命名
这种不饱和烃的总配方是 C n H 2n–2 ,其中 n–2,3,4,5……。根据 IUPAC 框架,烯烃的名称有一个后缀-yne,前缀取决于碳颗粒的数量。炔烃的一些名称如下: 2 C2H2 Ethyne 3 C3H4 Propyne 4 C4H6 Butyne 5 C5H8 Pentyne 6 C6H10 Hexyne 7 C7H12 Heptyne 8 C8H14 Octyne 9 C9H16 Nonyne 10 C10H18 DecyneNumber of carbon atoms Formula IUPAC name
炔烃中的异构现象
炔烃的结构异构如下:
- 链异构:由于不同的碳链构型,链异构发生在具有五个或更多碳原子的炔烃中。举个例子,
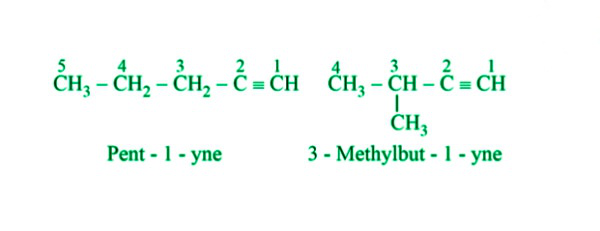
链异构
- 位置异构:在这种情况下,异构体的三键位置不同。丁烯的两种异构体,例如,
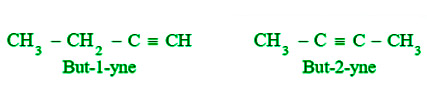
位置异构
- 功能异构:二烯有两个双键,而炔烃是二烯的功能异构体。

功能异构
- 环链异构:与环烷烃,炔烃显示环链异构。举个例子,
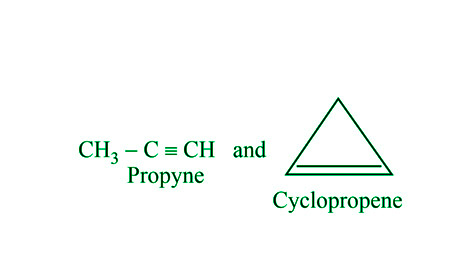
环链异构
炔烃的制备方法
以下是一些最常见的炔烃制备方法:
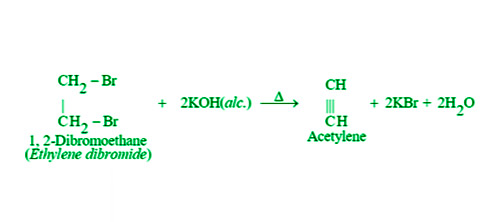
- 通过二卤代烷烃的脱氢:连位二卤代烷烃在氢氧化钾的醇溶液中的脱卤化氢可用于制备炔烃。举个例子,
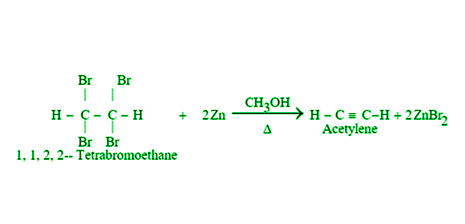
- 通过四卤化物的脱卤:当四卤代烷在甲醇中与锌粉一起加热时,它们会脱卤并产生炔烃。举个例子,
- 卤仿脱卤:氯仿和碘仿与银粉加热,脱卤生成乙炔。

- 由碳和氢合成:氢气蒸汽可以类似地用于制造乙炔,方法是将其通过在两个碳电极之间形成的电弧。 Berthelot综合是这种方法的名称。
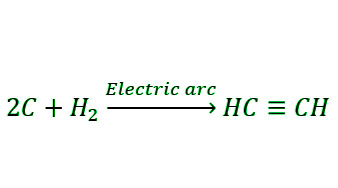
炔烃的物理性质
炔烃的性质与烷烃和烯烃的性质基本相似。
- 炔烃是不饱和碳,在碳位点具有三重安全性
- 所有的炔烃都是无味的,除了乙烯有轻微的特殊气味。
- 最初的三种炔烃是气体,后面的八种是流体。所有高于这十一个的炔烃都是固体
- 炔烃在性质上有些极性
- 炔烃的沸点和液化点随着它们的原子设计变得更大而增加。沸腾的边缘随着其亚原子质量的膨胀而增加
- 此外,炔烃的限制略高于其相关烯烃的限制,因为在碳位点有一个额外的键。
炔烃的化学性质
酸性性质
谈到炔烃的合成特性,我们从它们的微酸性开始。目前,炔烃本质上是微带负电的。炔烃中的三重强化碳颗粒是 sp 杂化的,而在烷烃中,单键 iotas 是 sp3 杂化的,导致电负性的区别。这使得它们更容易吸引 CH 键的公共电子对。因此,当我们用乙炔对像 NaNH2 这样的固体碱作出反应时,我们会得到乙炔钠和游离氢气 (H2)。然而,这种反应不会发生在烷烃和烯烃中。最终是炔烃中与碳碳三键相连的氢粒子在性质上有些酸性。值得注意的是,暴露这些氢粒子的其他氢粒子不是酸性的。
HC ≡ CH + Na → HC ≡ C– Na + + 1/2H 2
加成反应:
当情况合适时,炔烃会发生水合反应。当炔烃与卤素、氢和其他类似元素反应时,它们会产生一个饱和分子。两个氢原子、卤化物或卤素可以添加到它们的结构中,因为它们包含一个三键。
- 添加二氢:使用镍、铂或钯等催化剂来加速该过程。当将氢添加到炔烃中时,我们得到烯烃。
C 3 H 4 (g) + 2H 2 (g) → C 3 H 8 (g)
- 卤素的加成:当炔烃与氯等卤素反应时,卤素与炔烃的结构键合,生成卤素取代的烯烃。四氯乙烷将成为最终产品。
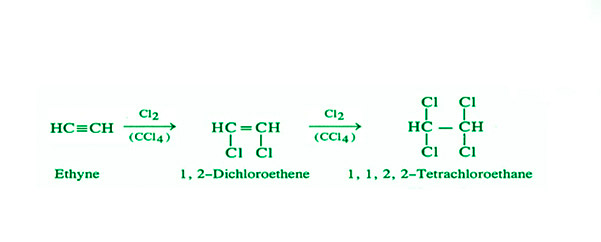
添加卤素
- 加水:炔烃不像其他碳氢化合物(烷烃和烯烃)那样与水分子发生反应。这被称为不相容性。当炔烃在催化剂硫酸汞存在下通过稀硫酸(约 40%)鼓泡时会发生反应。羰基分子将是这个过程的最终产物,这个过程被称为水合反应。
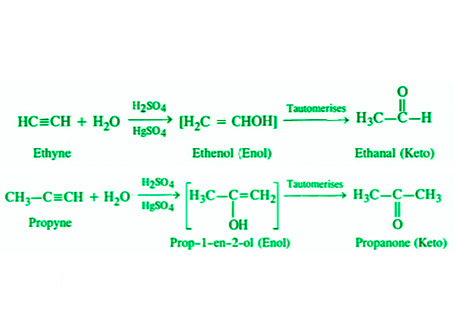
加水
- 聚合:在适当的情况下,炔烃可以进行线性和环状聚合。发生聚合,产生分子量大于初始炔烃的分子。例如,乙炔将聚合产生聚乙炔或聚乙烯(具有更大的分子量)。循环聚合需要高温和催化剂的存在。就像将乙炔在至少 877K 的温度下通过炽热的铁管生产苯一样。
炔烃的用途
- 由于乙炔具有异常炽热的火焰,因此通常用于氧乙炔气焊和氧乙炔气割。当乙炔被氧气点燃时,已知随后的火灾温度约为 3600 开尔文。
- 乙炔中的替代炔烃被用作燃料,每年通过部分氧化气态汽油产生大量公斤。使用这些炔烃的一部分生产物质混合物,例如乙醇腐蚀剂、丙烯酸腐蚀剂和乙醇。
- 乙炔最常用于制造天然混合物,如乙醇、乙醇腐蚀剂和丙烯酸腐蚀剂。它还用于为它们制造聚合物和原材料。
- 乙炔被分成两部分,碳和氢。这种反应会产生大量的热量,无论是否存在空气或氧气,都可以使气体变轻。
- 炔烃大部分用作组装大量具有机械意义的天然混合物(如氯丁二烯、氯乙烯等)的起始材料。
示例问题
问题1:什么是炔烃?
回答:
In natural science, alkynes are the unsaturated hydrocarbons having something like a triple connection between carbon-carbon particles (– C≡C–). The overall recipe of this unsaturated hydrocarbon is CnH2n–2, where n–2,3,4,5… … .
Alkynes are customarily known as acetyls. Like different hydrocarbons, alkynes are additionally hydrophobic.
问题2:炔烃的性质是什么?
回答:
The first three alkynes are colourless gases, the next eight are liquids, and the higher alkynes are solids. They are odourless, insoluble in water but soluble in organic solvents due to their non-polar nature, have high melting and boiling temperatures, and are lighter than water.
问题3:炔烃的主要用途是什么?
回答:
Acetylene, often known as ethyne, is the most common alkyne chemical. The following are a few examples of applications:
- In gas welding, an oxyacetylene flame is employed.
- Hawker’s lamp and lighthouses both employ acetylene as an illuminant.
- Acetylene is used to make fruits ripen artificially.
- Acetylene is used to make acetaldehydes, acetic acid, ethyl alcohol, synthetic rubber, and other valuable chemicals.
- In organic chemistry, acetylene and its derivatives are commonly employed to make cis and trans alkenes, methyl ketones, and other compounds.
问题 4:炔烃本质上是酸性的吗?
回答:
Alkynes have a small negative charge. This is due to the sp hybridization of the triple linked carbon atoms in alkynes, which makes it simpler for them to attract the shared electron pair. Alkyne molecules can readily lose hydrogen as a result. As a result, the acidity of the hydrogen atom connected to the triple bound carbon atom.
问题5:为什么炔烃的沸点更高?
回答:
The melting and boiling temperatures of alkynes rise as the molecular mass of the alkynes increases. Alkynes, on the other hand, have greater melting and boiling points than alkanes and alkenes. This is due to the fact that alkynes are linear and their molecules are packed closer together in space.
问题6:炔烃是如何制备的?
回答:
Chlorine or bromine is mixed with an inert halogenated solvent like chloromethane to produce a vicinal dihalide from an alkene. To make an alkyne, the produced vicinal dihalide is heated and reacted with a strong base.
问题 7:我们如何将炔烃还原为烯烃?
回答:
Alkynes can be transformed to trans-alkenes by dissolving sodium in an ammonia solution. A Na radical gives an electron to one of the P bonds in a carbon-carbon triple bond. This produces an anion in an ammonia solution, which may be protonated by a hydrogen.