乙酸——结构、性质、用途、示例问题
碳是生命存在所必需的非金属。这个名字来自拉丁词“carbo”,意思是“煤”。这是因为它是煤炭最重要的组成部分。从化石燃料到复杂分子,碳是大多数有机材料中含量最丰富的化学物质。二氧化碳仅占大气的 0.03%,地壳仅含有 0.02% 的矿物形式的碳。尽管碳在自然界中的含量非常低,但它的重要性似乎是巨大的:碳化合物存在于化石燃料、聚合物、肥皂、清洁剂和我们使用的大部分药物中。
乙酸
Ethanoic acid (also known as acetic acid) is a two-carbon acid that follows methanoic acid as the second member of the carboxylic acid family (which is a one-carbon carboxylic acid).
尽管乙酸是该酸的正确且技术上合法的 IUPAC 术语,但其流行名称乙酸经常被用作其 IUPAC 名称。醋是一种流行的家用产品,由 5-8% 的乙酸水溶液制成。它通常用于厨房。乙酸在整个冬天都会结冰,呈现出冰川的外观;因此,它也被称为冰醋酸,是一种流行的实验室化学品。
乙酸的结构
乙酸的化学式为 CH 3 COOH,其缩合形式也可以写成 CH 3 CO 2 H 或 C 2 H 4 O 2 。它的分子量为 60.05 g/mol(或摩尔质量)。
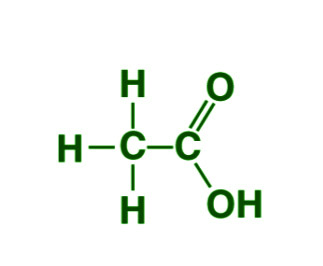
乙酸的结构
在甲醇之后,乙醇具有第二简单的羧酸结构。羧酸官能团 (-COOH) 与甲基 (-CH 3 ) 基团相连。有人认为乙酰基 (-CH 3 CO) 和羟基 (-OH) 之间的连接是其结构的原因。可见与 sp 2的杂交。由于两个乙酸分子之间发生分子间氢键,它通常以液态和气态的二聚体形式存在。电负性较小的氢原子的电子云吸引羧酸基团的电负性较大的氧原子,建立氢键。
乙酸的物理性质
- 纯乙酸是一种无色透明液体,具有独特的气味。
- 乙酸的燃点为 39°C。
- 乙酸的厚度为1.05 g/cm 3 。
- 乙酸的极限为 118°C,其软化点为 16°C。
- 乙酸有一个氢键受体和两个氢键受体。
- 在 25°C 时,纯乙酸在水中的溶解度 >100 mg/mL。它推断它在所有程度上都可深度溶解在水中。
- 乙酸完全溶于天然溶剂,例如四氯化碳和二硫化碳。可与乙醚、苯、CH 3 )2CO、甘油和乙醇等天然溶剂混溶。
- 乙酸的烟雾菌株在 25°C 时为 15.7 mm Hg。
- 乙酸的 LogP 为 – 0.17。
- 乙酸在普通实验室储存温度和不同条件下大体上是稳定的。
- 乙酸的厚度在 25°C 时为 1.056 mPa-s。
- 乙酸的表面压力在 25°C 时为 27.10 mN/m。
- 乙酸的着火热为 874.2 kJ/mol。
- 乙酸的汽化热在 25°C 时为 23.36。
- 1.0 摩尔排列的乙酸的 pH 值为 2.4。
- 乙酸的 pKa(分离稳定性)在 25°C 时为 4.76。
乙酸的化学性质
- 酯化反应:当羧酸与醇相互作用时,它会产生酯,这是一个新的化学分子家族。酯化是产生酯的化学过程。当乙酸(一种羧酸)与乙醇(乙醇)结合时,会形成如下所示的乙酸乙酯(一种酯):
CH 3 COOH + CH 3 CH 2 OH → CH 3 COOCH 2 CH 3
这种反应产生了一类新的化合物,具有独特的果味,使其易于识别。酯类在食品行业中用作合成调味剂,在香水行业中因其令人愉悦的香味而被使用。除此之外,酯类最常见的用途之一是制造肥皂。当酯与任何碱(尤其是碱)反应时,会形成羧酸盐,这是soap的基本分子结构。皂化反应是这个过程的名称。该反应最好用较高分子量的酯进行。以下是皂化反应的广义解释:
RCOOR' + NaOH → RCOO–Na + + R'OH
- 与碱的反应:酸性乙酸是一种弱酸。它与碱相互作用产生一分子盐和一分子水,就像任何其他酸一样。乙酸与氢氧化钠(一种碱)反应生成乙酸钠和水,如下所示:
CH 3 COOH + NaOH → CH 3 COONa + H 2 O
这种盐(乙酸钠)具有多种工业应用,包括在纺织工业中中和硫酸(用于清洁纤维),在食品工业中作为防腐剂和温和的调味剂和调味剂,以及作为乙醇的缓冲剂酸(通常称为醋酸盐缓冲液)以维持介质的 pH 值。
- 与碳酸盐的反应:当乙醇与碳酸盐或碳酸盐的氢衍生物(碳酸氢盐,也称为碳酸氢盐)反应时,会形成盐作为副产物,以及二氧化碳和水。
2CH 3 COOH + Na 2 CO 3 → 2CH 3 COONa + CO 2 + H 2 O
乙酸的制备方法:甲醇的羰基化是获得乙酸的最常用技术。在羰基金属作为催化剂存在下,甲醇与一氧化碳反应生成乙酸。
乙酸的用途
- 它在需要非质子溶剂的各种工艺中用作溶剂。
- 醋、酯和合成聚合物都是由它制成的。
- 它在实验室中用作血细胞的裂解剂。
- 它用于治疗真菌感染。
- Soap的制造:将动物脂肪或植物油(橄榄油、蓖麻油或棕榈油)与氢氧化钠或氢氧化钾一起加热制成soap。要制作soap,请用强氢氧化钠溶液加热脂肪或植物油,直至形成soap和甘油。皂化反应是制造soap过程的名称。甘油是该过程的一种有价值的副产品,因为它用于制造各种化合物、炸药和药物。

示例问题
问题1:soap的化学名称是什么?
回答:
Sodium stearate is the sodium salt of stearic acid, a long-chain saturated fatty acid (C17H35COOH). The lengthy alkyl chain C17H35 and the ionic carboxylate group COO–Na+ are found in sodium stearate.
问题 2:当乙酸与乙醇反应时会发生什么?
回答:
Ethanol combines with ethanoic acid to form a fruity-smelling molecule known as ethyl ethanoate, which is an ester. Esterification is the name given to this process.
问题3:乙醇和乙酸的气味是什么?
回答:
Ethanol is a flammable, volatile, colourless liquid with a pleasant odour, whereas ethanoic acid is a colourless liquid with a strong vinegar-like odour.
问题4:乙酸有什么用途?
回答:
The uses of Ethanoic Acid are:
- It’s utilised as a solvent in a variety of processes that call for a protic solvent.
- Vinegar, esters, and synthetic polymers are all made from it.
- It is used in labs as a lysing agent for blood cells.
- It is used to treat fungal infections.
问题5:soap的清洁作用是什么?
回答:
Oily or greasy compounds are not wettable by water. However, the soap anion’s hydrocarbon residue R (RCOO–) can do so.
When a filthy cloth is dipped into a soap solution owing to the deposition of dust, oil, or greasy substances, the hydrocarbon non-polar portion R (hydrophobic) of the RCOO– ion dissolves as polar impurities of oily or greasy dirt and encapsulates it in the micelle. The micelles that transport the oily or greasy particles are washed away when the fabric is cleaned with water.