第 16 族 p 嵌段元素 – 氯族
p-block元素的价(最外层)电子都在 p 轨道中,将它们联合起来。 p 轨道由六个叶状结构组成,它们从中心点均匀辐射。因为 p 轨道只能携带六个电子,所以 p-block 分为六列。第 13 列有一个 p 轨道电子,它是 p 块的第一列。在第 14 列(p 块的第二列)的元素中可以找到两个 p 轨道电子。直到第 18 列,它有六个 p 轨道电子,趋势继续朝这个方向发展。
氯
氯是一种化学元素,原子序数为 17,符号为 Cl。它是仅次于氟的第二大电负性元素,平均原子质量为 35.453 amu。 1774 年,瑞士-德国化学家 Carl Wilhelm Scheele 通过将盐酸与氧化锰 (IV) 结合,率先分离出这种元素。
但直到 1810 年,戴维才得出结论,舍勒创造了元素氯。氯气的名字来源于希腊语“chloros”,意思是“黄绿色”。
因为氯是元素周期表卤素族中的第二个元素,所以它的性质主要介于氟和溴之间。在环境温度下,它是一种黄绿色气体,以双原子分子 Cl 2的形式自然存在。在这种排列中,两个氯原子可以共享它们最外层的轨道电子,形成共价键。

二氯甲烷
氯的位置
氯在元素周期表中被列为第 17 位元素。它位于第三阶段和第 17 组。
氯的发生
在地壳和海水中都可以找到大量的氯。氯作为分子氯化钠 (NaCl) 的一部分存在于海洋中,也称为食盐。它是地壳中的石盐、光卤石和钾盐中的矿物。
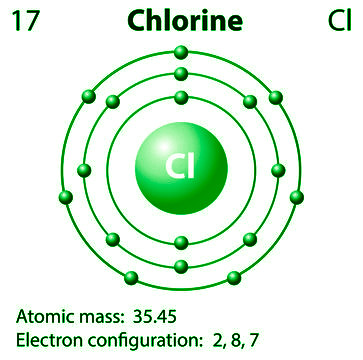
氯的原子结构
氯的原子序数为 17,这意味着它有 17 个质子和 17 个电子围绕原子核运行。根据电子分布,电构型为2、8、7。这意味着 7 个电子位于最外层的 M 壳层中。结果,氯原子有七个价电子和一个价。此外,根据壳分布,其电子分布为 1s 2 2s 2 2p 6 3s 2 3p 5 。
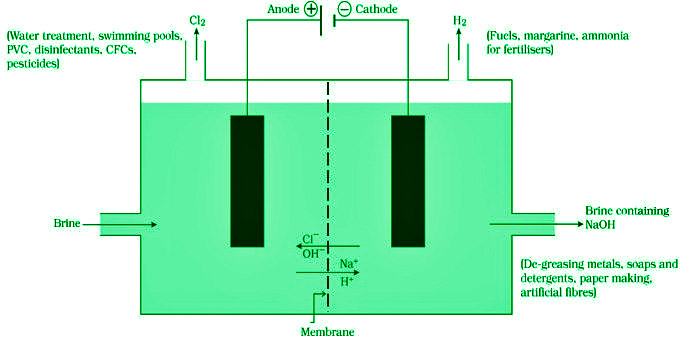
氯气的制备
有几种替代方法可用于大规模生产氯。以下是一些最常用的方法:
- 氯碱法是一种生产氯化钠水溶液的工业方法。在阴极产生氢气,在阳极产生氯气,而在电解液中产生氢氧化钠。
- 氯化氢的氧化是迪肯的方法。在 723K 的温度下,与空气或氧气混合的气态氯化氢在与作为催化剂的氯化铜接触的浮石上移动。
4HCl+O 2 →2Cl 2 +2H 2 O
氯的性质
物理性质
- 它是一种强烈的刺激性气体,外观呈黄绿色,带有刺鼻、难闻的气味。
- 它是非爆炸性和不易燃的。
- 氯是在正常条件下形成双原子分子的气体。
- 它的重量是空气的 2.5 倍。
- 在水中,它有些溶解。
- 它的沸点为239.11摄氏度,熔点为171.6摄氏度。在室温下,它很容易通过冷却或几个大气压的压力液化。
- 较重、电负性较小的卤素溴和碘被氯从化合物中置换出来。
化学性质
- 氯气微溶于水,遇潮气生成次氯酸(HClO)和盐酸(HCl)。
- 当金属与氯反应生成Ionic氯化物时,就会形成离子氯化物。例如。 – 2Na+Cl 2 →2NaCl
- 与有机物质的反应——氯与多种有机分子反应生成氯化衍生物。一些反应,特别是那些涉及碳氢化合物、醇和醚的反应,可能非常剧烈。
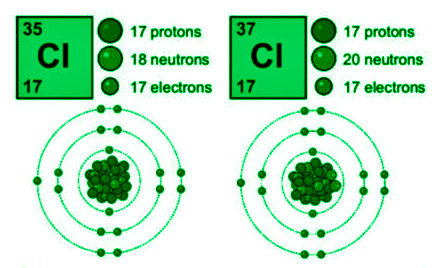
氯的同位素
同位素是具有相同原子序数并且在元素周期表中处于相同位置但由于其原子核中的中子数量不同而具有不同质量数的两种或多种类型的原子。
氯有两种稳定同位素: 35 17 Cl (75.77%) 和37 17 Cl (37.77%),原子量为 35.45amu。
氯的用途
- 作为消毒剂:氯基消毒剂通过杀死可能导致腹泻、游泳者耳朵和脚癣等皮疹等疾病的细菌来使水安全。
- 作为漂白剂:氯用于生产家用氯漂白剂,可对衣物进行增白和消毒,以及对厨房和浴室表面进行消毒,并能有效消灭使人生病的细菌。
- 作为杀虫剂:它用于制造多种杀虫剂,保护农作物免受昆虫侵袭。
- 工业:用于制造纸张和纸制品。它用于生产聚合物和染料。
- 药品:用作防腐剂和药品生产。
一些有趣的事实
- 第一次世界大战期间,德国人用氯气毒死盟军士兵。
- 氯原子约占海洋体积的 1.9%,以盐水的形式存在。
- 氯气的密度是空气的 2.5 倍。
- CFC 或氯氟烃由氯制成,以前通常用于空调和喷雾罐。然而,由于它们导致臭氧层的消耗,现在主要被禁止。
- 含有溶解氯化钠的水的电解用于生产工业中使用的大部分氯气(盐水)。
氯对人体有什么作用?
氯中毒:氯是一种抑制水中微生物生长的化学物质。接触、吞咽或吸入该物质可能会导致氯中毒。它与水结合,在体内和体外的粘膜表面产生盐酸和次氯酸,包括我们消化道中的水。人类可能会被这两种酸中毒。
- 咳嗽、呼吸困难和肺部积液都是呼吸道症状。
- 口腔灼热、喉咙痛、胃痛、呕吐、便血都是消化系统的征兆。
- 血液 pH 值平衡的变化、严重的眼部损伤以及由烧伤和刺激引起的组织损伤导致的皮肤损伤都是循环系统的迹象。
示例问题
问题一:氯对人体有什么作用?
回答
Chlorine is a chemical that inhibits the growth of microorganisms in water. Chlorine poisoning can be caused by touching, swallowing, or inhaling the substance. It combines with water to produce hydrochloric acid and hypochlorous acid on mucosal surfaces both within and outside the body, including the water in our digestive tract. Humans can be poisoned by both of these acids.
- Coughing, difficulty breathing, and fluid in the lungs are all respiratory symptoms.
- Burning in the mouth, throat pain, stomach pain, vomiting, and blood in the faeces are all indications of the digestive system.
- Changes in the pH balance of the blood, severe eye injury, and skin damage resulting from tissue injury with burns and irritation are all signs of the circulatory system.
问题2:氯是用来做什么的?
回答
The following are some of the applications of chlorine:
- As a disinfectant, for starters.
- It’s a bleaching agent that’s used in both households and businesses.
- It’s used to make polymers and dyes, among other things.
- It’s utilised in the manufacture of insecticides.
- It’s used to make a variety of compounds, including hydrochloric acid.
- It is utilised in the manufacturing of pharmaceuticals.
问题 3:氯的配方是什么?
回答
The chemical formula for Chlorine is Cl2.
问题 4:氯是 Cl 还是 Cl 2 ?
回答
Chlorine is a diatomic molecule with the formula Cl2. Two Chlorine atoms can share their outermost orbit electrons in this arrangement, forming a covalent link.
问题 5:氯是酸性还是碱性?
回答
Chlorine gas has neither acidic or basic properties. Because of the presence of hydronium ions in the solution, the chlorine aqueous solution is acidic.
问题 6:关于氯的三个有趣的事实是什么?
回答
The following are three fascinating facts about chlorine:
In the oceans, chlorine is the third most prevalent element. It is the human body’s tenth most prevalent element. Electrolysis on water containing dissolved sodium chloride is used to produce the majority of chlorine gas used in industry (saltwater).
We hope you found this Chlorine post useful. If you have any problems, please let us know in the comments box below and we will respond as quickly as possible.